
癌症液体活检作为一种能从体液中获取疾病分子信息的无创检测技术,已在多种癌症中得到广泛应用。然而,现行的医学临床液体活检技术均依赖于生物特异性修饰步骤,导致其成本高、耗时长,从而难以真正应用到全民癌症普筛之中。近年来,表面增强拉曼散射(SERS)凭借其高灵敏度的技术优势,已在癌症相关的应用场景中崭露头角。其中,标签SERS虽然具有高精度,但需要依赖生物特异性修饰;无标签SERS虽然成本低廉,但难以规避体液微环境的扰动等问题。因此,研发一种兼顾高精度和低成本的SERS技术,对其在临床医学中的应用具有关键作用,是目前的研究难点和热点。
基于上述问题,武汉大学肖湘衡教授、武汉大学中南医院汪付兵教授与电子科技大学胡婧研究员合作建立了一种以低廉银纳米线为SERS探针的无标签、液相光学检测体系,并借助人工智能深入进行后续数据分析和癌症预测(SERS-AICS),最终在实验中,我们针对五种不同癌症的血清样本(样本来自382例健康个体和1582例患者)的精准普查(平均准确率高达95.81 %、平均灵敏度高达95.40 %、平均特异度高达95.87 %),通过进一步的临床实验,该技术有望进行I/II期癌症与癌前疾病的早期筛查(平均准确率高达88.39 %)。
这项技术有望用于低成本、快速且精准的全民癌症筛查。更重要的,该研究发现血样中通过降维获得的拉曼特征维度与癌症密切相关,且反映了更为微观的分子键能层面变化,这使SERS-AI有望成为一种涵盖已知癌症大分子标志物、甚至预测未来潜在癌症标志物的全光谱组学数据库来源(图1)。

图 1:SERS-AI助力高精度的血清泛癌筛查及早筛示意图
该文章发表在卓越计划高起点新刊eLight上,题目为“Early cancer detection by serum biomolecular fingerprinting spectroscopy with machine learning”。
在获取样本SERS光谱数据信息后,研究团队首先选取五种癌症中样本量最大的肺癌(LC)样本进行SERS-AI分析,以8:2的比例划分训练集及测试集,再借助二分类SVM分类器可成功将244个LC样本和324个健康对照组(HC)样本从训练集和内部测试集中区分开来,对应的LC/HC模型鉴别肺癌患者与健康对照的受试者工作特征ROC曲线下面积 (AUC) 为0.90 (图2A)。基于SERS-AI对于血清的识别分类具有良好的普适性,研究团队进一步成功地将其推广到结直肠癌(CRC)、胃癌(GC)、肝癌(HCC)、食管癌(ESCA)甚至是混合组(Mix)的血清体系分析中 (图2B-F)。针对癌症样本与正常样本,所有数据集都展现出令人满意的区分度,其混淆矩阵显示其对癌症样本判定的总体准确率、灵敏度、特异性分别高达为95.81 %、95.87%、95.40% (图2G-I)。
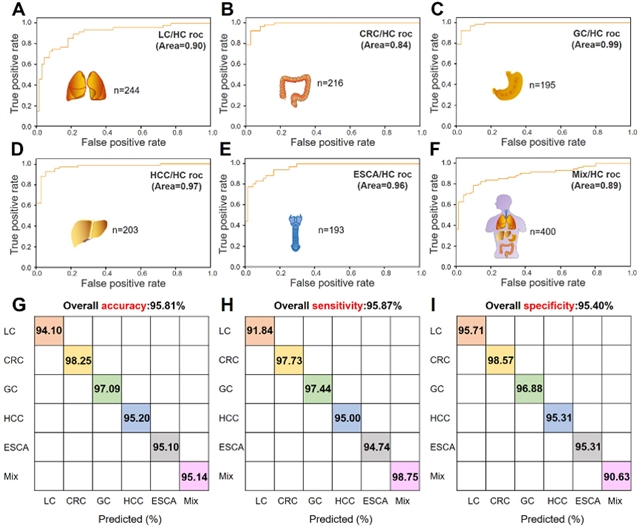
图2:基于SERS-AICS的五种高死亡率癌症筛查
此外,癌症早筛对于患者的生存率具有重大意义,因此研究团队也致力于利用SERS-AI技术将I/II期癌症样本与相关组织其他疾病的样本有效区分。研究结果表明肺、结直肠、胃、肝脏相关的常见疾病组/早期癌症组均具有良好的模型拟合度(图3B-E),并对早期癌症的识别具有较高的准确性、敏感性和特异性。其中,该技术对胃、肝相关数据集具有最佳的识别效果,对应准确率为93.33 %和92.31 %,敏感性为100 %和85.71 %,特异性为85.71 %和100 % (图3F)。因此, SERS-AICS系统极具潜力发展为针对无症状人群进行有效筛查,防止其发展为晚期癌症的新兴检测手段。
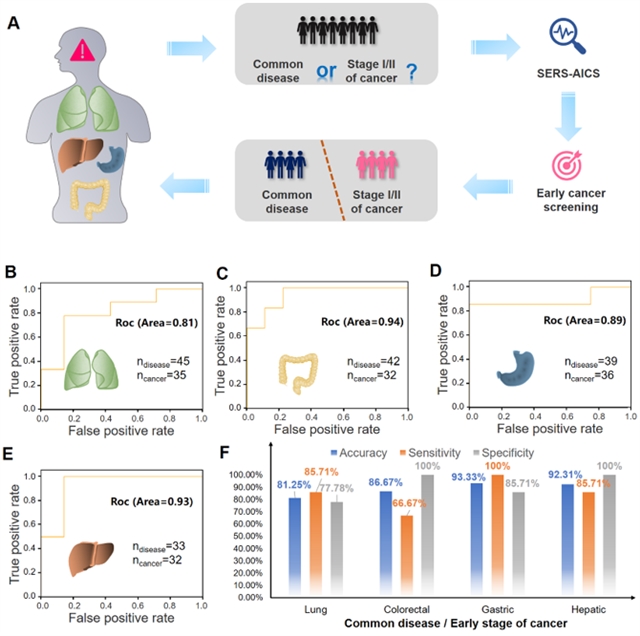
图3:基于SERS-AICS对四种代表性癌症进行早期筛查
目前,癌症筛查的发展还受到另一个限制,那就是缺乏数据库来存储、构建和追踪大量癌症患者的个体特征,从而制约了后续各项深入的本质分析,比如寻找新的癌症生物标志物的共同特征。根据上述测试及分析,SERS-AICS检测/分析系统共收集和处理了1964份血清样本,而且相比健康对照组,其对5种癌症的鉴定具有很高的准确性、灵敏度和特异性。同时,本项研究利用协方差矩阵辅助支持向量机分类策略在分析接近2000例的大样本血清拉曼数据时展现了独特的优势。这表明SERS-AICS可从五种代表性癌症中获得更可靠的光谱数据,进一步为未来的癌症普查提供了重要指导依据(图4A)。
更重要的是,SERS-AICS通过协方差矩阵降维,不仅可以简化模型构筑难度,也能够获取癌症相关的拉曼标志性维度(图4B)。基于上述与癌症相关的特异性维度的归属统计分析,可以计算出单独5种类型癌症、不同类型癌症任意混合组合、以及早期癌症与相应组织常规疾病之间的共享拉曼峰位置(图4C),并可在未来继续从中分析各类癌症的共同特征。与目前的单分子生物标志物相比,这些拉曼特征维度涵盖了样本中所有分子振动光谱的信息,对各种因癌症导致的微小变化的鉴定更为精细和准确。这表明在未来的癌症标志物探索中,SERS-AI数据库极有可能成为关联光谱和生物分子特性的重要信息来源。
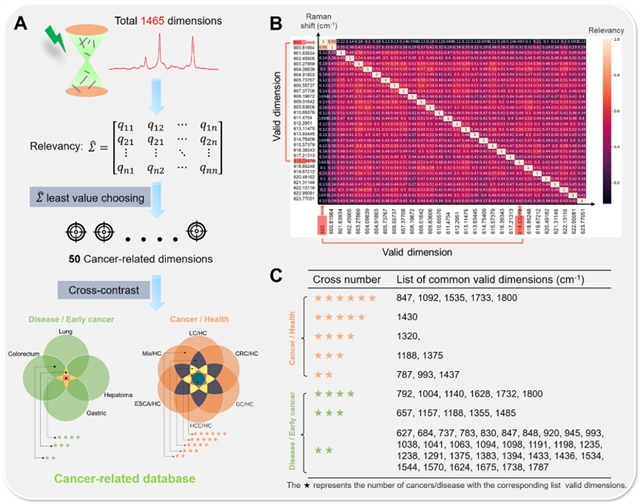
图4:通过SERS-AICS构建癌症相关数据库。(A)协方差矩阵将1465维降至50维;(B)维度挑选时的相关性热力图;(C)分子键能层面的癌症共有维度列表,星星越多证明此特征维度适用于更多癌症类型
综上,SERS-AICS技术将为高风险人群和癌症患者通过常规血检,提供一种精准高效低成本的癌症检测方式,可以作为影像学等癌症确诊测试的前期初步筛查手段。研究团队未来将努力推动SERS-AICS应用扩展到各种类型的癌症早筛,并且延伸到癌症患者确诊、治疗和复查等整个过程,并期望最终建立一个大规模数据记录、检索和研究的系统,为后续深入研发奠定坚实的基础。(来源:中国光学微信公众号)
相关论文信息:https://doi.org/10.1186/s43593-023-00051-5
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。