|
|
| 生物酶在金电极/纳米自组装膜的直接电子转移 | MDPI Catalysts |
|
论文标题:Direct Electrochemical Enzyme Electron Transfer on Electrodes Modified by Self-Assembled Molecular Monolayers(生物酶在金电极/纳米自组装膜的直接电子转移)
期刊:Catalysts
作者:Xiaomei Yan, Jing Tang, David Tanner, Jens Ulstrup and Xinxin Xiao*
发表时间:14 December 2020
DOI:10.3390/catal10121458
微信链接:
https://mp.weixin.qq.com/s?__biz=MzI1MzEzNjgxMQ==&mid=2649977123&idx=1&sn=
4448cd4613d7b013557262cb461681fc&chksm=f1decbe7c6a942f16d5ab0e39b8c03ff10
f84fdb857a4c64c6eef84d57664092c4c09c5675a0&token=1158289035&lang=zh_CN#rd
期刊链接:https://www.mdpi.com/journal/catalysts
原文通讯作者简介

肖鑫鑫
丹麦技术大学
肖鑫鑫博士于2019年1月在爱尔兰利莫瑞克大学 (University of Limerick) 获得自然科学博士学位,现就职于丹麦技术大学(Technical University of Denmark)化学系,担任研究员。在Chemical Reviews、 Journal of the American Chemical Society等期刊发表学术论文40篇。
曾获2019年度爱尔兰皇家科学院Kathleen Lonsdale Prize (青年化学家奖),2019年度国际电化学学会 (ISE)“青年电化学家旅行奖”,2020年度CSC国家优秀自费留学生奖学金。
主要研究方向:生物电化学
研究背景
生物酶在电极表面的直接电子转移 (Direct Electron Transfer, DET) 是生物传感器和生物燃料电池等生物电化学器件的基础。纳米自组装膜(Self-Assembled Monolayer, SAM) 可以自发有序地在金、铂、银等金属表面形成。自组装膜分子具有广泛可选择的的碳链长度、终端基团等,这便使得金电极/纳米自组装膜界面具备很好的可控性,并成为用来研究生物酶直接电子转移的理想基底。
近期,来自丹麦技术大学化学系的NanoChemistry团队在Catalysts期刊上综述了金电极/纳米自组装膜的制备和基本表征,对可进行直接电子转移的常见生物酶 (蛋白) 进行了总结和归类,讨论了生物酶在金电极/纳米自组装膜的直接电子转移。
综述内容
酶在电极上的直接电子转移,指的是氧化还原酶(催化过程中有电子的参与) 的催化活性中心可以直接跟固态电极表面建立起电子联系。这是依靠电子隧穿实现的,故需要酶的活性中心距离电极表面足够近,一般要小于2纳米。所以,具有单一活性中心的酶,若其活性中心距离酶的表面远大于2纳米的话,则无法进行直接电子转移。最典型的例子就是原生的葡萄糖氧化酶 (Glucose Oxidase, GOx) 是无法进行直接电子转移的。
很多酶分子在催化活性中心外,还具有一个或多个电子转移中心 (Electron Transfer Relay),如铁基的血红素 (Heme) 等。因酶的底物被氧化 (或者被还原) 而产生的电子在酶分子内部可以从活性中心转移到电子转移中心,从而进一步转移到电极表面。该综述文章总结了常见的可以实现直接电子转移的酶,并根据电子转移中心进行了分类(图1)。具体来说:(1) 含有血红素的酶,如Cytochrome (cyt,是一种蛋白,不是酶), Fructose Dehydrogenase (FDH), Cellobiose Dehydrogenase (CDH), Glucose Dehydrogenase (GDH)和 Sulfite Oxidase (SOx)等;(2)含有铜原子的酶,如Azurin, Copper Nitrite Reductase (CuNiR), Bilirubin Oxidase (BOD)和Laccase (Lac)等;(3) 含有[FeS]团簇的酶,如基于[FeFe]-, [NiFe]-, [NiFeSe]的Hydrogenase等。
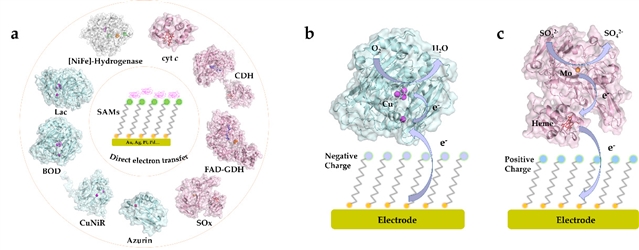
(a) 常见的可以实现直接电子转移的酶;(b) 催化氧气还原的bilirubin oxidase;(c) 催化亚硫酸盐氧化的sulfite oxidase的直接电子转移示意图
为了使得酶的电子转移中心距离电极表面足够近,需要调节酶在电极表面的构象,这是生物 (电) 催化剂和无机 (电) 催化剂 (如铂纳米颗粒) 的根本不同。铂纳米颗粒本身具有很好的导电性,可以直接跟支撑电极实现很好的电子转移。不同的酶具有截然不同的表面特性 (亲疏水性、正负电荷),这是由表面的氨基酸序列决定的。因此,电极表面也需要进行化学修饰而实现酶在电极上的合理构象。自组装膜可以使得电极表面具有不同的特性,从而到达上述目的。
该综述文章对每一种酶的电子转移路径、表面特性都进行了详细的描述,并给出了合适的自组装膜的选择建议。
特刊推荐
Enzymatic Bioelectrocatalysis
♦ Edited by Elisabeth Lojou and Xinxin Xiao
♦ Submission Deadline31 March 2021
Link:https://www.mdpi.com/journal/catalysts/special_issues/enzy_bioelect
Catalysts(ISSN 2073-4344; IF 3.520) 是一个国际型开放获取期刊,期刊主题涵盖催化剂和催化反应等各个相关领域的研究。Catalysts目前已被SCIE、Scopus、Inspec (IET)等重要数据库收录。Catalysts采取单盲同行评审,文章平均处理周期一个月左右,一审周期约为11天,文章从接收到发表仅需2.9天。


特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。