|
|
| NK细胞激活型受体分子DNAM-1及其与配体互作机制研究取得进展 |
|
人体内环境的稳态是机体进行正常生命活动的必要条件,而机体的免疫系统则是维持机体稳态的重要调节机制。在免疫系统中,自然杀伤(Natural killer, NK)细胞是一类由造血干细胞发育分化而来的淋巴细胞亚群,是天然免疫和细胞免疫的生力军。它能够释放穿孔素和颗粒酶直接介导靶细胞的坏死和凋亡,同时也通过释放多种细胞因子调节T、B淋巴细胞等多种免疫细胞功能,最终达到免疫监视和免疫稳态的目的。
NK细胞的功能受细胞表面“阴”、“阳”两类受体分子的协调控制。配对的抑制型受体和激活型受体能够识别相同的MHC-I类分子。由于抑制型受体与配体的亲和力较高,NK细胞通常处于抑制状态。病毒感染等刺激信号会导致激活型受体过表达,竞争性结合配体,激活NK细胞,使其“杀死”进入体内的病原微生物或清除体内不断出现的自身病变细胞。
近年来,一类新发现的配对的NK细胞受体家族逐渐走入人们的视线,这就是由抑制型受体TIGIT、CD96和激活型受体DNAM-1(CD226)组成的TIGIT-CD226-CD96受体家族。该受体家族分子通过特异性地识别相同配体——nectin/Necl家族分子CD155(Necl-5),调控NK细胞功能。TIGIT更是作为一种抑制型免疫检查点分子,被广泛应用于各种靶点细胞治疗的研究和临床应用当中。DNAM-1是该家族中唯一的激活型受体分子。因此,对DNAM-1与其配体的作用机制的研究,不仅能够阐明其激活NK细胞的作用机制,而且对以DNAM-1为靶点的免疫治疗性药物的开发具有重要价值。
最近,PNAS (《美国科学院院报》)报道了中科院微生物所高福院士团队关于DNAM-1与配体CD155互作机制的重要研究成果。
研究团队解析了人DNAM-1和小鼠DNAM-1分子的胞外段高分辨率三维结构。通常而言,具有多个Ig样结构域的蛋白,其Ig样结构域间通常形成一种“头尾相接”的串联方式(见CD155分子)。这种“念珠”样的排列导致相邻两个Ig结构域之间具有一定的柔性,便于其通过构象调整而结合受体/配体分子。研究人员发现,由两个V型免疫球蛋白(IgV)结构域构成的DNAM-1分子,其两个IgV结构域呈现独特的“肩并肩”的并排排列模式。这种特殊的串联方式使得两个结构域的β片层(β-sheet)通过氢键网络连接成一个“刚性”的整体,从而产生了一种 “超级免疫球蛋白 (super-Ig)”结构域。类似的排列模式仅见于文昌鱼的免疫类似分子VCBP3(variable-region containing chitin-binding protein 3)的结构中。研究人员推测,这种Ig结构域之间“肩并肩”的刚性排列可能会对其功能产生一定影响,而这种特殊的排列模式对于理解免疫球蛋白这类古老的免疫分子的进化规律提供了新的线索。
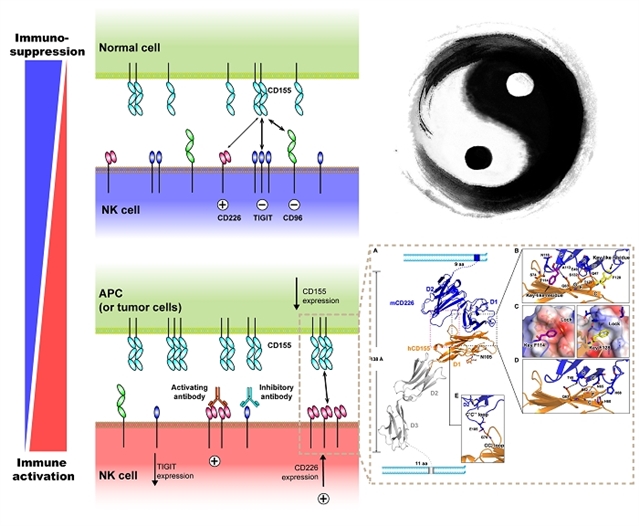
DNAM-1/CD226与配体CD155分子互作对NK细胞的活化具有重要作用
研究团队还系统地研究了DNAM-1分子与其配体CD155分子的结合机制。通过对DNAM-1/CD155复合物结构的解析,他们发现DNAM-1主要通过远膜端的IgV(CD226-D1)结构域与CD155分子的远膜端的IgV(CD155-D1)结构域通过“双锁钥(double-lock-and-key)”的结合模式进行结合。而后,通过对DNAM-1不同结构域截短体蛋白及突变体蛋白与CD155结合能力的检测,他们发现DNAM-1近膜端IgV(CD226-D2)结构域不仅在维持CD226分子的整体构象稳定性上具有重要作用,同时更直接参与了与CD155分子的互作。这种特殊的结合模式在TIGIT-CD226-CD96家族分子与配体的结合中前所未见。
研究人员同时发现,激活型受体DNAM-1与配对的抑制型受体TIGIT对于配体CD155的结合能力处于同一水平。这个结果提示,TIGIT-CD226-CD96家族对于NK细胞功能的调控可能不同于以往所知的“抑制信号优先”的调控模式。
综上所述,文章对DNAM-1与其配体的作用模式的阐明,对于理解TIGIT-CD226-CD96家族受体分子与配体的作用机制以及NK细胞的调控机制具有重要意义。同时,该研究对于开发以DNAM-1为靶点的肿瘤免疫治疗性抗体药物提供了重要的理论基础。
近年来,研究团队在T细胞及NK细胞关键受体/配体作用机制及肿瘤免疫检查点抗体药物作用机制方面开展了系列工作,在nectin/Necl家族分子与病毒表面抗原及免疫相关受体分子互作机制方面的研究成果相继发表在Nature Structure and Molecular Biology、PLoS Pathogens、Structure、Journal of Immunology和Journal of Virology等杂志,为理解这类分子在免疫调控及病原入侵方面的作用机制及药物开发提供了重要基础。
中国科学院北京 研究院博士后王寒为论文第一作者,中国科学院微生物研究所高福院士和谭曙光副研究员为论文共同通讯作者。本研究得到了国家自然科学基金、中国科学院战略性先导科技专项项目以及博士后创新人才支持计划的经费支持。(来源:中国科学院微生物研究所)
论文连接:https://doi.org/10.1073/pnas.1815716116
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。