导读
光动力治疗(Photodynamic Therapy,PDT)是一种依赖光敏剂、特定波长光照和分子氧协同作用的肿瘤治疗方式,具有空间选择性强、对正常组织损伤小等优势,近年来,随着光纤与内窥镜技术的发展,PDT 已逐步从体表肿瘤拓展至结肠、食管等实体瘤治疗领域
然而,肿瘤微环境复杂、血管异常、基质致密,使得传统给药方式难以将足量光敏剂输送至肿瘤深部,从而削弱治疗效果。如果药进不了肿瘤,再好的光也没用。这是光动力治疗(PDT)发展几十年来始终绕不开的现实问题。目前,PDT 的临床疗效始终受到关键问题的限制——光敏剂在肿瘤组织中的有效累积不足。
针对这一核心挑战,斯科尔科沃理工学院Olga A. Sindeeva团队提出了一种基于巨噬细胞介导递送的光动力治疗新策略。主要利用巨噬细胞天然的肿瘤归巢能力,搭载逐层自组装(LbL)微胶囊递送光敏剂,构建 "特洛伊木马" 式治疗体系,展现了提升结肠癌光动力治疗效果的巨大潜力。该研究成果发表在 Light: Advanced Manufacturing,题目为Macrophage-mediated delivery of microcapsules for enhanced photodynamic therapy of colon cancer 。
小百科:什么是“LBL微胶囊”?
LbL微胶囊: 逐层自组装(layer-by-layer, LbL)技术通过交替沉积带相反电荷的材料,在模板上构筑多层薄膜,形成中空微胶囊载体。LbL 微胶囊的优势是结构稳定、负载能力强、壳层可设计调控,且中空、可变形结构有利于细胞吞噬与组织迁移。LbL构建的微胶囊可封装药物,具有药物控释、延长体内循环和提高生物利用度的优点,为靶向药物释放提供平台。
核心设计:LbL 微胶囊 + 巨噬细胞,打造高效递送系统
研究团队以 6.2±0.5μm 的球霰石颗粒为模板,交替沉积三种不同的聚电解质对(PAH/PSS、BSA/TA、PArg/DS),形成中空 LbL 微胶囊,再将两种第二代光敏剂 ——Photoditazine(PD)和铝四磺化酞菁(PS)封装其中。
随后,利用巨噬细胞对肿瘤组织的天然趋化性,让其主动捕获载药微胶囊,形成 "巨噬细胞 - 微胶囊 - 光敏剂" 递送复合体,精准靶向肿瘤部位,在 660nm 红光照射下触发光敏反应,产生细胞毒性单线态氧,实现肿瘤杀伤,如图1所示。
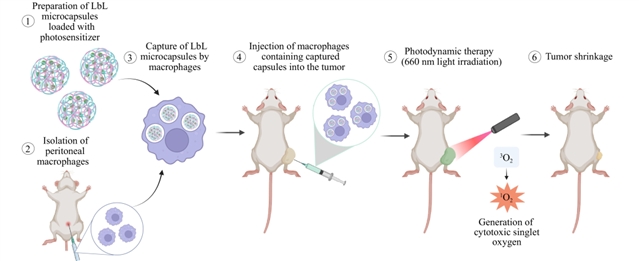
图1:巨噬细胞介导递送微胶囊的PDT示意图
关键验证:从体外实验看系统优势
1. 游离光敏剂安全性与有效性双重保障
实验在 CT-26 结肠癌细胞、RAW 264.7 巨噬细胞及 L929 成纤维细胞中验证了两种光敏剂的性能,如图2所示:
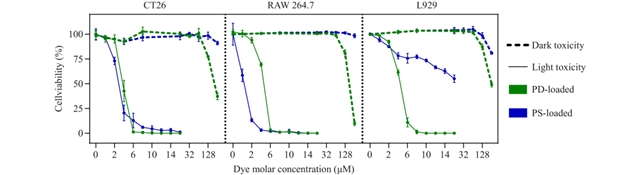
图2:光敏剂在不同细胞系中的光/暗毒性
结果显示在低浓度下均表现出极低的暗毒性(无光时无明显损伤),而在 660nm 红光照射下,能高效诱导肿瘤细胞凋亡,其中 PD 在 6μM、PS 在 10μM 浓度下可实现 CT-26 细胞近 100% 死亡,兼具安全性和治疗活性。
2. 微胶囊性能优化:筛选最优载体
分别通过 zeta 电位、荧光成像、药物释放等检测发现:
BSA/TA 涂层微胶囊因药物释放过快、荧光信号易淬灭被排除,如图3所示;PAH/PSS 和 PArg/DS 涂层微胶囊能有效保留光敏剂,且兼容性良好;其中(PArg/DS)?微胶囊表现最佳,不仅载药量高达 14pg / 胶囊,在巨噬细胞内可稳定存在长达 6 天,未观察到明显结构破坏,为长效治疗提供可能。

图3:球霰石颗粒的SEM表征及负载光敏剂的微胶囊共聚焦成像
3. 巨噬细胞选择:原代细胞更胜一筹
对比两种巨噬细胞的递送能力发现:
RAW 264.7 巨噬细胞主要将微胶囊保留在细胞表面,内吞效率低;
原代腹腔巨噬细胞(PMs)可在 3 小时内高效内吞微胶囊,且能携带微胶囊迁移至肿瘤球内部,实现光敏剂的深度递送。
4. 体内验证:结肠癌模型中显疗效
在 CT-26 结肠癌小鼠模型中,研究团队设置 5 组对照实验(每组 9 只小鼠):①对照组、②单纯巨噬细胞组、③单纯微胶囊组、④巨噬细胞 + 微胶囊组、⑤游离光敏剂组,经瘤内注射后 24 小时给予 660nm 激光照射。如图4,15 天后结果显示:
第④组实验中肿瘤重量中位数仅 8.1mg,4/9 小鼠实现肿瘤完全消退;
第⑤组虽有 2/9 小鼠肿瘤消退,但整体抑瘤效果稍弱;
第①/③组肿瘤生长抑制不明显。
这一结果表明,巨噬细胞介导的递送方式有望提升光敏剂在肿瘤内的生物利用度,有效克服传统 PDT 药物分布不均的问题。
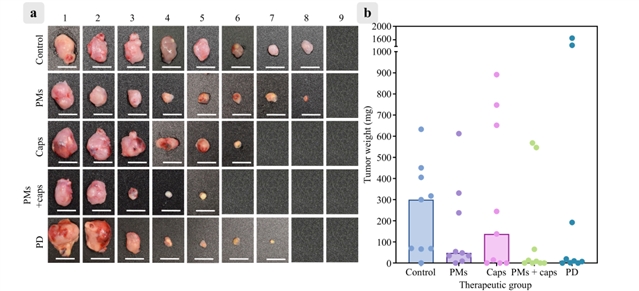
图4:光动力疗法后相同组别的肿瘤大小及重量分布图
展望
该研究成功将巨噬细胞的肿瘤归巢能力与 LbL 微胶囊的载药优势相结合,为实体瘤 PDT 提供了新策略,但仍需解决三大挑战:
大体积肿瘤中光敏剂递送深度和均一性需进一步优化;
巨噬细胞长期携带微胶囊的功能稳定性及免疫调控影响需系统评估;
临床转化需解决细胞来源标准化、载药一致性等工程问题。
未来通过优化微胶囊结构、联合免疫调控策略及个体化细胞递送方案,该体系有望发展为高精度、低副作用的实体瘤治疗新平台,为结肠癌等难治性实体瘤患者带来新希望。(来源:先进制造微信公众号)
相关论文信息:https://doi.org/10.37188/lam.2026.002
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。