
化学成像可以针对基础 研究以及临床诊断提供关键信息,是生物医学的一个重要研究分支。传统化学成像,普遍依赖于荧光标记物与特定细胞结构结合的方式提供信息。然而,由于荧光标记物会对生物样本造成干扰,如何实现无标记化学成像获得了学界广泛的关注。相干拉曼散射(coherent Raman scattering),是近年来蓬勃发展的一种无标记化学成像技术。这种”选键“成像利用激光控制细胞内自身的分子震动,可以在微秒内获取分子的化学键信息,从而实现无标记活体生物成像。相干拉曼成像在过去十余年内获得了长足进展,然而,受制于拉曼散射截面的物理极限,一些瓶颈制约了该技术的进一步提高。
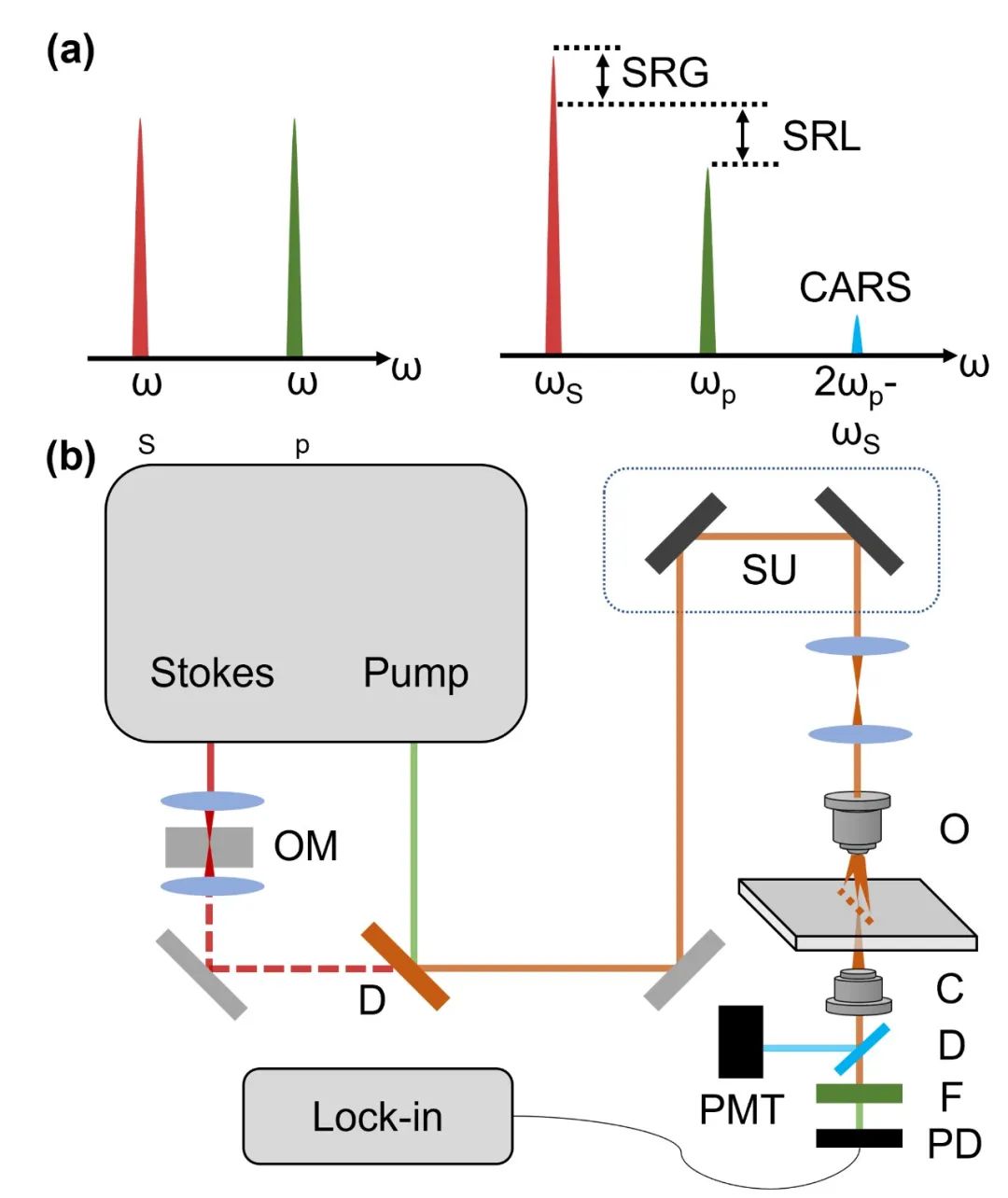
图1:相干拉曼原理示意图
计算光学成像 (computational imaging),是结合光学系统优化与图像信号处理的新兴领域。通过利用图像数据的特定性质,前端系统可以进行特殊采样设计,从而实现对特定物理极限的突破。例如,压缩感知成像利用图像信号本征的稀疏性质,可以利用随机欠采样的数据恢复出无损信号。近年来,越来越多的计算光学方法被提出,使其在功能(三维成像,散射重建,相位,光场,光谱)及性能(成像速度,空间分辨率,灵敏度,空间带宽积延拓)上突破传统极限。
作为两个新兴领域的交汇,计算相干拉曼成像是突破无标记化学成像极限的有力途径,获得了国内外科研工作者的广泛关注。来自波士顿大学的程继新教授和林浩楠博士后在卓越计划高起点新刊eLight发表综述“Computational coherent Raman scattering imaging: breaking physical barriers by fusion of advanced instrumentation and data science”,总结了该方向的的进展和未来趋势。
文章首先讨论了利用压缩感知提高相干拉曼成像速度的相关工作。相较于传统压缩感知二维宽场成像,相干拉曼具有以下两点主要区别:首先,相干拉曼需要点扫描成像(类似双光子)以保持信号强度,其次,为了区分细胞内不同化学键的分子,相干拉曼通常会采用超光谱(hyperspectral)采样。基于以上两点,科研人员们设计出多种随机欠采样方式,提高了约一个数量级的成像速度。其中包含了光谱域利用空间光调制器随机调制,空间光谱联合随机点扫描采样,以及时间域随机采样并进行傅里叶变换。得益于高光谱数据在空间以及光谱域的冗余性,科研人员利用约20% 的采样率重建出完整信号,实现了约一个量级的成像速度提升。
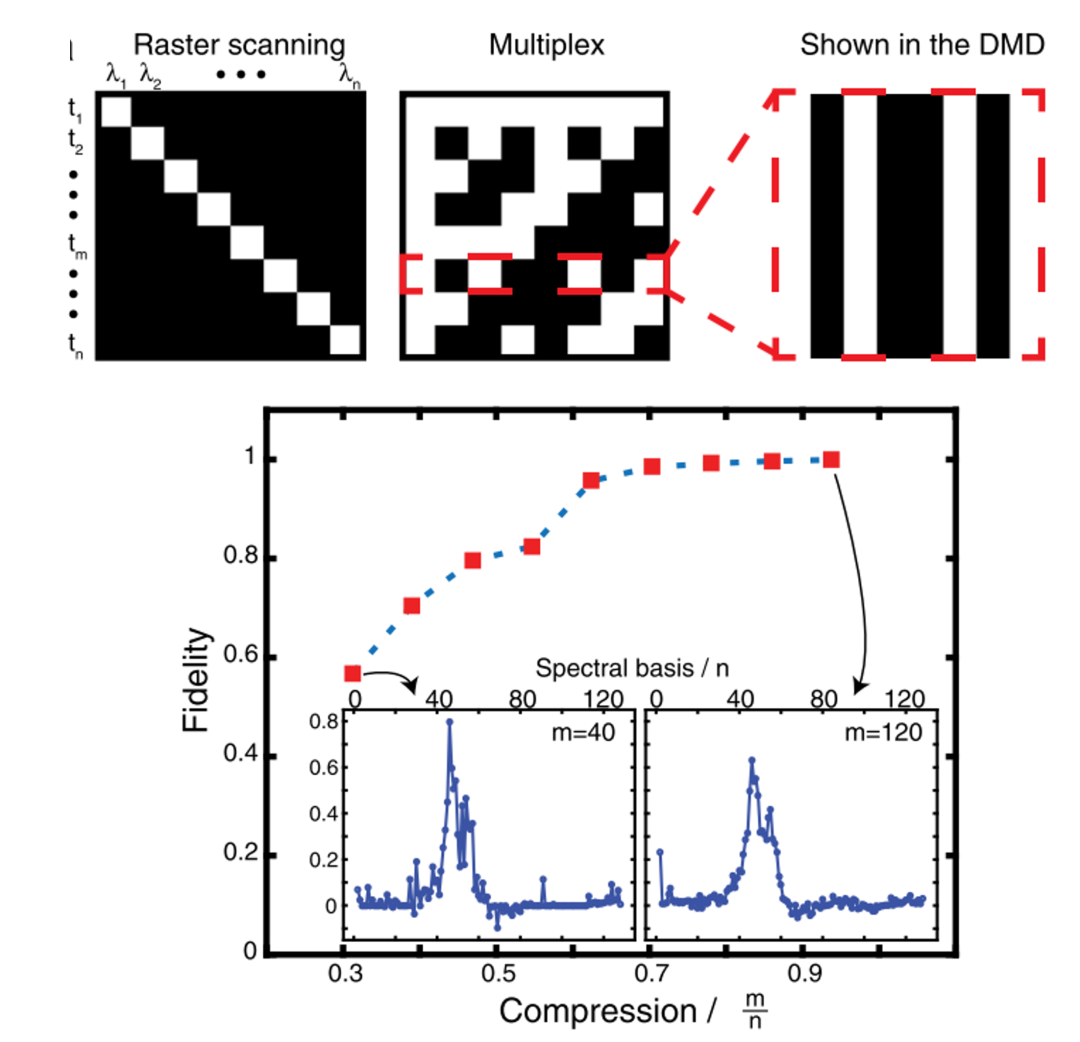
图2:压缩感知在超光谱相干拉曼中的应用
作为计算成像的另一重要分支,高速三维成像也在相干拉曼成像中得到了广泛重视。其中,数字全系成像是一种利用两束光干涉,通过相位记录样品三维信息的手段。在相干反斯托克斯拉曼散射(coherent anti-Stokes Raman scattering)中,研究人员通过额外引入一束参考光的方式实现了宽场离轴全系成像。此外,基于点扫描方式,投影层析成像也被利用到了相干拉曼领域。为了记录三维空间信息,研究人员使用了样品旋转,离轴激发,以及空间频率调制激发等不同手段,均实现了高速细胞三维成像,为进一步活体研究铺平了道路。
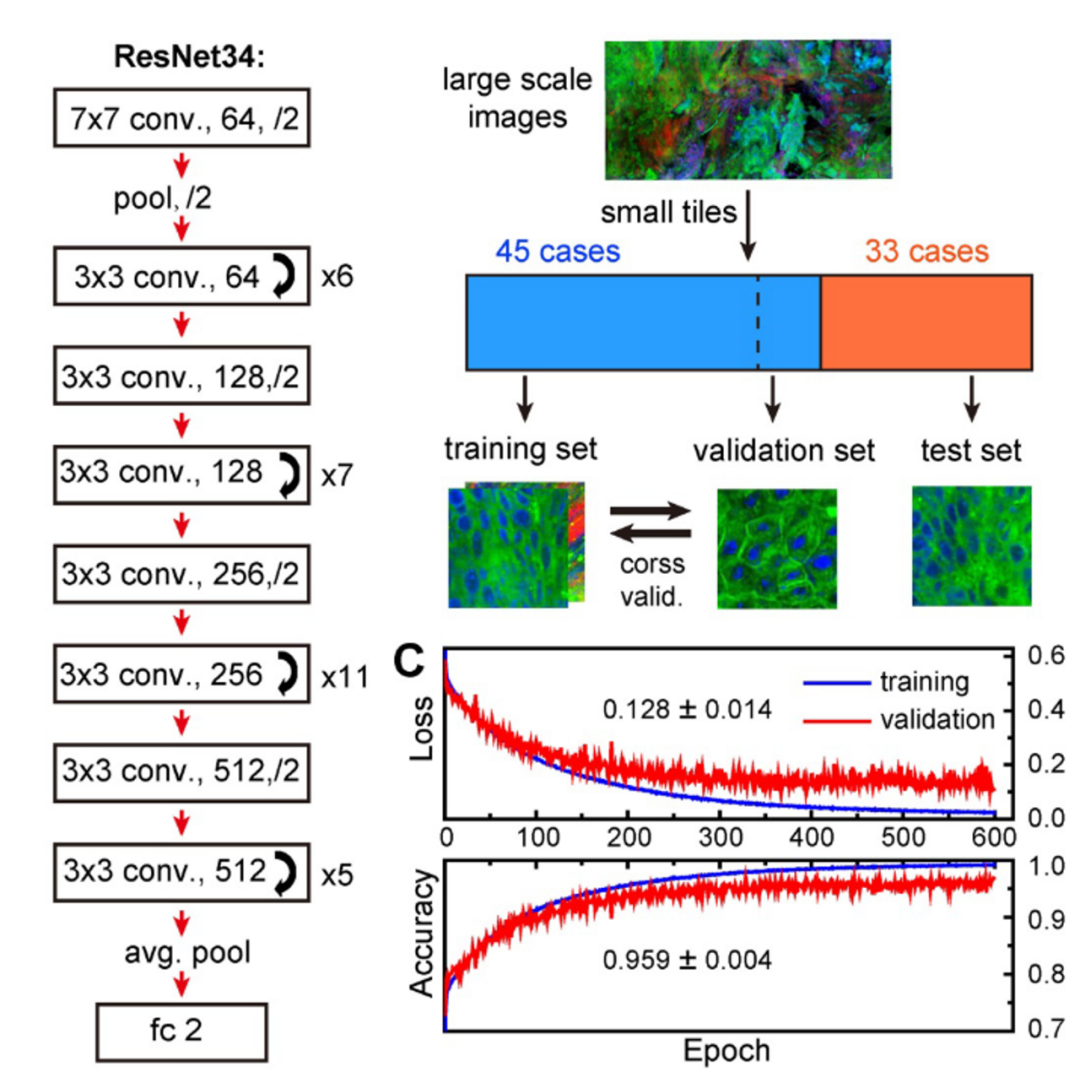
图3:相干拉曼投影层析成像
此外,深度学习在近年来蓬勃发展,解决了大量传统解析算法无法建模的问题,使得计算光学如虎添翼。深度学习在相干拉曼中得到了多样化的应用。深度学习图像降噪使得相干拉曼在灵敏度上得到了一个量级的提升。基于深度学习的医学图像识别,使得相干拉曼能够在手术中实时检测病灶。同时,深度学习也被用于非线性背景的去除以及跨成像模式的细胞结构预测,实现了功能以及性能的提高。

图4:深度学习在相干拉曼图像识别中的应用
随着光学元件,探测器以及算法的不断进步,计算光学成像在将来会发挥更重要的作用。由于其普适性,现有的计算相干拉曼手段能够继续提高系统性能。而针对空间分辨率,成像深度,空间带宽卷积的计算成像新方法也会随着光学硬件系统的不断升级而浮出水面。
相关论文信息:https://doi.org/10.1186/s43593-022-00038-8
(来源:中国光学微信公众号)
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。