香港中文大学的杨英洋教授团队与沙特阿卜杜拉国王科技大学的黄国维教授团队合作在Chem期刊上发表了一篇题为“Cross-assembly confined bifunctional catalysis via non-covalent interactions for asymmetric halogenation”的新研究。
课题组利用非共价作用来组装非手性路易斯碱和手性磷酸形成限域的双功能催化剂。通过改变非手性路易斯碱催化剂,可以对催化剂口袋进行精细调节,避免了传统的手性双功能催化剂冗长的合成步骤,从而提高了不对称反应优化的效率。利用此策略实现了溴鎓离子引发的高对映选择性的半频哪醇重拍和分子内醚化反应。
论文通讯作者是郑添裕、黄国维、杨英洋;第一作者是郑添裕、陈锐。
手性双功能性催化剂可以提供一个限域的环境来实现高对映选择性的反应。但是通常需要冗长的合成步骤来引入不同的取代基去调节限域的微环境,这会降低优化反应的效率。手性磷酸是在不对称反应中最通用的双功能性催化剂,许多高对映选择性的反应可以通过改造手性磷酸的取代基来实现。然而合成不同的手性磷酸通常需要早期引入不同的取代基,这意味着需要大量的平行合成降低了效率。
杨英洋研究团队一直致力于不对称卤代反应的研究(Nature Catalysis2020, 3, 993-1001;Chem2020, 6, 919-932;J. Am. Chem. Soc.2021, 143, 12745-12754;J. Am. Chem. Soc. 2014, 136, 5627-5630;J. Am.Chem. Soc. 2013, 135, 1232-1235;J. Am. Chem. Soc. 2011, 133, 9164-9167;J. Am. Chem. Soc. 2010, 132, 15474-15476)。不对称卤代反应通常需要手性双功能性催化剂来实现,例如手性磷酸。然而改造手性磷酸催化剂通常需要大量的时间且低效,有时甚至需要特殊的大位阻卤代试剂才能实现高对映选择性的卤代反应。通过近期对催化反应中的非共价作用的研究(ACS Catal. 2019, 9, 8083-8092;ACS Catal. 2021, 11, 3498-3506;),该团队设想可以通过非共价作用来组装手性磷酸和非手性的路易斯碱催化剂构造新型的手性双功能性催化剂以提高不对称卤代反应的优化效率(图1)。

图1:非共价作用组装形手性双功能性催化剂用于不对称卤代反应。
为了验证该设想,溴鎓离子引发的半频哪醇重拍被选为模板反应,杨英洋课题组与黄国维课题组合作通过密度泛函理论计算以及二维核磁实验验证了环丙烯硫酮作为非共价作用的供体,与N-溴代丁二酰亚胺(NBS)和手性磷酸混合后,通过非经典氢键的作用可以形成C1对称的手性复合物,并且此催化的活性位点比单独的手性磷酸更加限域(图2)。
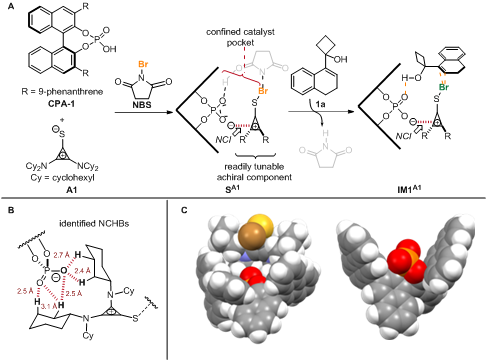
图2:通过非共价作用组装的催化模式。
通过改变不同的非手性路易斯碱催化剂,利用环丙烯硒酮A4与CPA-1,可以得到97% e.e.的重排产物2a。通过改变非手性路易斯碱,利用氨基吡啶来调节催化口袋的大小,该体系还可以应用到不对称溴代分子内醚化反应中。溴代呋喃4a具有97.5:2.5的对映选择性,并且通过密度泛函理论计算,提出的通过非经典氢键组装的中间体SB2是热力学合理的(图3)。
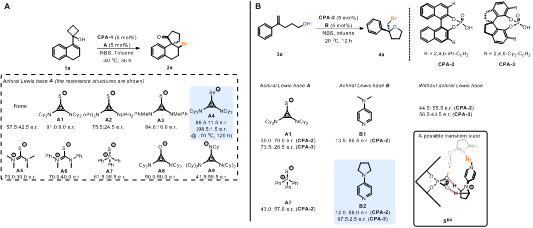
图3:通过改变非手性路易斯碱催化剂优化反应。
发展的不对称溴代分子内醚化反应可以应用到天然产物的全合成以及药物中间体的合成当中(图4)。
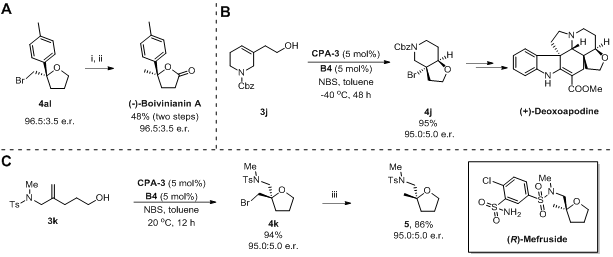
图4:天然产物及药物中间体的合成。
该研究通过利用非共价作用组装手性磷酸与非手性路易斯碱形成新的双功能性催化体系,通过主要筛选非手性路易斯碱催化剂实现了不同的不对称卤代反应。该项研究为设计手性双功能性催化剂提供了新思路。(来源:科学网)
相关论文信息:https://doi.org/10.1016/j.chempr.2023.01.016