|
|
|
|
|
中外科学家合作开发新型仿生免疫调控策略治疗慢性牙周炎 |
|
|
2021年9月14日,上海交通大学医学院刘尽尧教授、陆尔奕教授团队与哈佛大学陶伟教授团队合作在Cell姊妹刊Matter在线发表了一篇题为“Biomimetic immunomodulation by crosstalk with nanoparticulate regulatory T cells”的新研究。
本研究开发了基于调节性(Treg)细胞膜包覆纳米颗粒的仿生免疫调控策略,这一人造纳米Treg细胞通过与靶细胞的直接接触而发挥多重免疫调控作用,从而有效减缓了慢性牙周炎的进展。刘尽尧教授、陆尔奕教授和陶伟教授为该论文共同通讯作者,上海交通大学医学院李双博士为第一作者。
过度激活的免疫反应在自身免疫性疾病和慢性牙周炎等众多免疫炎症性疾病的发生发展中起到关键作用。在不同组织部位,多种活化的免疫细胞所介导的复杂免疫反应通常都会进一步引发扩大级联的复杂炎症反应,从而导致组织的持续损伤和疾病的不断进展。目前对于这些免疫炎症性疾病的治疗,一方面主要通过抗炎药物的使用来对抗下游的炎症反应,但是由于这种策略通常只针对复杂炎症网络中的少数靶点起作用,因此疗效也较为有限;而另一方面通过广谱免疫抑制性药物的使用来抑制上游过激的免疫反应的方法则因其全身副作用大等缺点而应用受限。因此,针对免疫过度活跃相关疾病的新治疗策略的开发是目前需要亟待解决的问题。
调节性T(Treg)细胞是一类控制体内自身免疫反应性的T细胞亚群,它对于机体免疫稳态的维持具有重要作用。值得注意的是,Treg细胞除了通过分泌抑制性细胞因子来发挥抑制作用外,还能通过与多种免疫细胞的直接接触来调控其免疫激活状态。而在病灶组织中如慢性牙周炎局部,Treg活细胞的免疫抑制表型常因组织局部丰富的炎症因子作用而受损。因此本研究受到Treg细胞生物学功能的启发,开发了基于Treg细胞膜包覆聚乳酸-羟基乙酸共聚物(PLGA)纳米颗粒(TNPs)的仿生免疫调控策略,为免疫炎症性疾病的治疗提供新策略和新思路(图1)。
研究结果表明这一人造纳米Treg细胞具有Treg活细胞表面的功能性膜蛋白,因此它能够特异性地粘附于单核巨噬细胞表面并上调其吲哚-2,3双加氧酶(IDO)的表达而促进其凋亡,最终抑制了单核巨噬细胞的破骨分化;它还能够与树突状细胞表面的共刺激分子的直接相互作用而抑制其成熟。值得注意的是,TNPs还能粘附于活化T细胞周围而抑制其增殖与细胞因子分泌功能。这些实验结果表明TNPs可以通过与多种靶细胞之间发生直接串扰而发挥多重免疫调控作用。
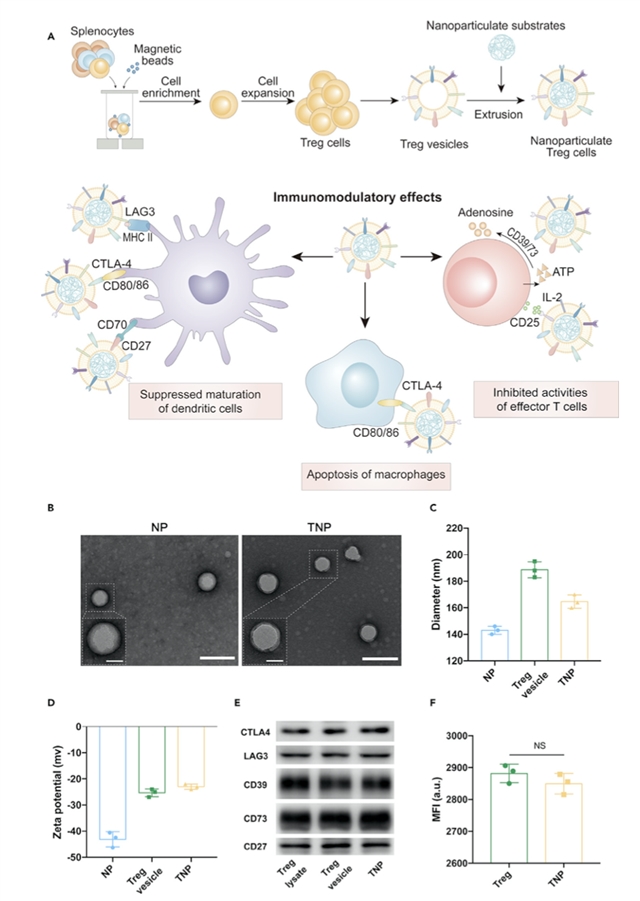
图1:TNPs的制备、理化表征及其多重免疫调控作用
在小鼠早期和晚期牙周炎动物模型中,TNPs能够显著抑制牙周炎局部和引流淋巴结中的CD4+ T细胞的过度激活,同时还能够有效缓解牙周组织炎症并减缓小鼠牙槽骨的吸收(图2)。在比格犬慢性牙周炎模型中,TNPs仍然呈现出显著的炎症抑制作用和牙周组织保护作用,有效抑制了慢性牙周炎的进展(图3)。
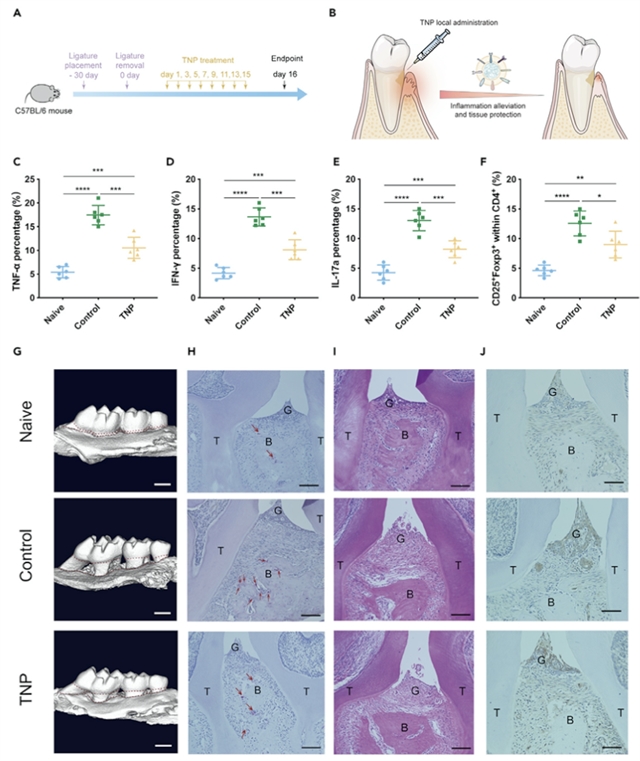
图2:TNPs在小鼠牙周炎模型中的免疫调控作用,抗炎及组织保护疗效
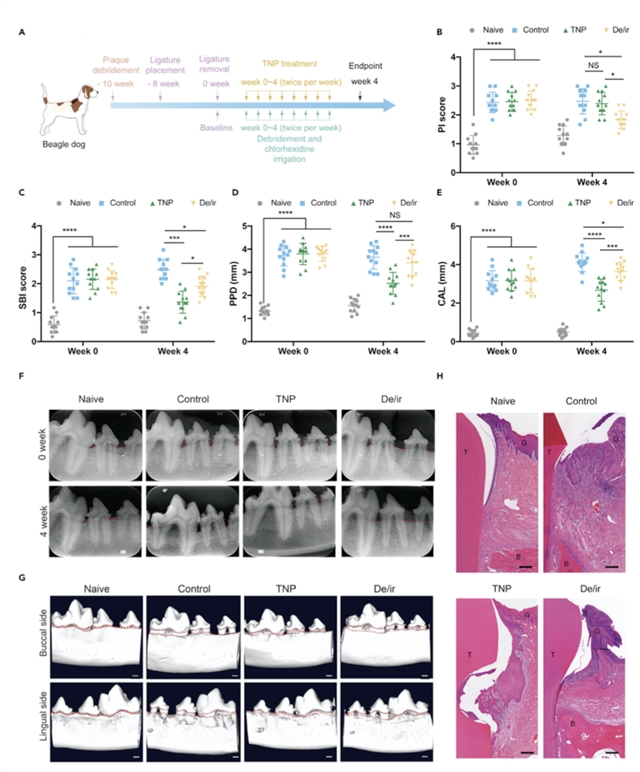
图3:TNPs有效缓解比格犬慢性牙周炎的进展
该研究工作获得国家自然科学基金委、上海市科学技术委员会、上海市教委和上海交通大学等资助。(来源:科学网)
相关论文信息:https://doi.org/10.1016/j.matt.2021.08.015