|
|
| 中国科学院长春应用化学研究所贺超良与陈学思团队:聚氨基酸水凝胶用于顺铂的局部释放 | MDPI Polymers |
|
论文标题:Injectable Click Polypeptide Hydrogels via Tetrazine-Norbornene Chemistry for Localized Cisplatin Release
期刊:Polymers
作者:Zhen Zhang, Chaoliang He and Xuesi Chen
发表时间:10 April 2020
DOI:10.3390/polym12040884
微信链接:
https://mp.weixin.qq.com/s?__biz=Mzg5MzU5MDkwMg==&mid=2247487463&idx=1&sn=
eed441e6414651426c42c67e2af783f9&chksm=c02dc3fef75a4ae8f63a13a369aa8c37b33
37544059aab59caeae034ab4f21ea6c597a7b37d6&token=2053333544&lang=zh_CN#rd
期刊链接:https://www.mdpi.com/journal/polymers
原文通讯作者简介
贺超良,博士,中国科学院长春应用化学研究所研究员、博士生导师。主要研究方向:仿生智能性高分子水凝胶的设计、制备与生物医学应用;抗肿瘤药物局部缓释载体材料;生物活性水凝胶组织再生与修复材料。已发表SCI论文100余篇;其中,以第一/通讯作者在多个影响因子大于5的SCI杂志发表论文40余篇。全部论文SCI他引总计5000余次,单篇最高SCI他引500余次,h-指数为45。以第一发明人获得授权中国发明专利17项。2013年入选中国科学院青年创新促进会 (2017年入选优秀会员)。2016年获得国家自然科学基金“优秀青年科学基金”。担任《中国科学:技术科学》中英文版青年编委。
陈学思,中国科学院院士,中科院长春应用化学研究所学术委员会常务副主任,中科院生态环境高分子材料重点实验室学术委员会副主任,生物高分子研究组组长,中共吉林省委和吉林省政府评为吉林省高级专家,享受政府特殊津贴。曾荣获中国科学院科技促进发展一等奖,中国化工学会“第六届侯德榜化工科学技术奖”,中国化学会“赢创化学创新奖”2014年 ,中国石油和化学工业联合会技术发明奖一等奖,“十一五”国家科技计划执行突出贡献奖,长春高新技术产业开发区管委会评为“自主创新十强企业”经营者,中国化学会高分子科学论文创新奖,长春高新技术产业开发区管委会评为科技创业先进个人,吉林省科技进步一等奖,世界华商创新奖“聚乳酸生物可降解材料”,国家杰出青年科学基金。长期从事高分子化学研究,设计与合成高旋光纯度的聚乳酸和聚氨基酸两大类聚合物,具体从事生物降解医用高分子材料与器件、组织工程支架和药物缓释载体、聚乳酸和聚ε-己内酯绿色材料产业化等方向的研究与开发工作。开展了PEG-g-聚谷氨酸/顺铂抗肿瘤纳米药物的制备及其应用研究。同浙江海正集团合作实现了1.5万吨聚乳酸产业化,技术水平达到了国际领先。组建了长春圣博玛生物材料有限公司,获得了可吸收骨折内固定钉和板CFDA两个注册证 (III类)。发表SCI学术论文700余篇,SCI他引2万余次,h-指数为83。授权专利260余项。近年来,主持国家自然科学基金基础科学中心项目及多项国家重点和重大科技项目。
顺铂 (CDDP) 是治疗各种上皮恶性肿瘤的一线化疗药物之一。然而,伴随的肾毒性、胃肠道毒性、周围神经病变和耳毒性等副作用严重危害病人健康。近几十年来,为了降低副作用,实现在肿瘤部位更高的药物浓度以及在较长的时间内可控的药物释放,人们研究开发了多种可控给药系统[1]。其中可注射的共价交联水凝胶系统由于其优越的机械性能和长期稳定性在药物递送方面得到了广泛的研究[2]。可注射水凝胶一般通过物理相互作用或共价键形成, 其中物理水凝胶可以在特别温和的条件下形成,但它们通常是机械强度与长期稳定性较低。共价键水凝胶具有良好的机械性能与稳定性,但是在交联反应过程中的副反应产物会具有细胞毒性,降低了水凝胶的生物相容性。因此,如何制备具有优异机械性能、长期稳定及良好生物相容性的水凝胶是一个关键难题。
成果简介
近日,中国科学院长春应用化学研究所张震博士、贺超良教授与陈学思教授在Polymers发表文章,报道了通过四嗪-降冰片烯的逆电子需求Diels-Alder (iEDDA) 点击反应制备了可注射聚氨基酸水凝胶用于顺铂的局部释放。该水凝胶药物缓释系统具有可控的机械性能,长期稳定并且具有良好的生物相容性,通过药物缓释结果亦证明该药物递送系统具有抗肿瘤作用并且降低了全身毒性。总体而言可注射点击聚氨基酸水凝胶在局部的持续肿瘤药物传递方面具有较大的潜力。
要点1:无铜点击聚氨基酸水凝胶的制备和表征
作者通过降冰片烯改性聚 (L-谷氨酸)(PLG-Norb) 和四嗪官能化四臂聚 (乙二醇)(4aPEG-T) 之间发生逆电子需求Diels-Alder (iEDDA) 点击反应制备可注射水凝胶,其中PLG-Norb 用于与 CDDP 形成聚合物-金属络合,药物释放过程在PBS中进行模拟,合成过程如方案1所示。
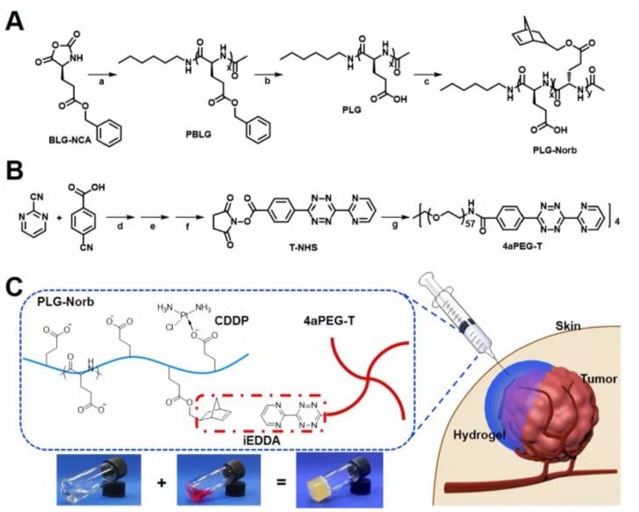
方案1:(A,B) 降冰片烯改性聚 (L-谷氨酸)(PLG-Norb) 和四臂聚 (乙二醇)(4aPEG-T) 的合成路线:a) 己胺,N,N-二甲基甲酰胺 (DMF),室温,72 小时;b) 氢溴酸,二氯乙酸,室温,2 小时;c) 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐 (EDC·HCl)、4-二甲氨基吡啶 (DMAP)、DMF,室温,72 小时;d) N2H4·H2O,乙醇,90℃,10小时;e) 亚硝酸异戊酯,乙酸,室温,过夜;f) EDC·HCl,N-羟基琥珀酰亚胺 (NHS),DMF,40℃,过夜;g) 二甲亚砜 (DMSO),50 °C,48 小时。(C) 用于局部治疗肿瘤的可注射点击聚氨基酸水凝胶的示意图。
为了研究交联过程中的流变行为,监测了水凝胶的 G´和 G´´随时间的变化。水凝胶的 G´随聚合物浓度和降冰片烯基团与四嗪基团的摩尔比 (表示为 [N]/[T]) 而变化。SEM 被用来检测冻干水凝胶的内部形态。如图1C所示,水凝胶具有高度多孔的网络结构,可能有利于药物运输。聚合物材料的降解是药物递送系统的主要问题。希望水凝胶在药物耗尽后降解以避免额外的手术去除载体。通过监测剩余质量来研究水凝胶在含有弹性蛋白酶的 PBS 中的体外降解行为。如图1D所示,水凝胶的质量在 6 天内不断减少,这应该归因于 PLG 主链的逐渐分解和随之而来的聚合物网络的降解。
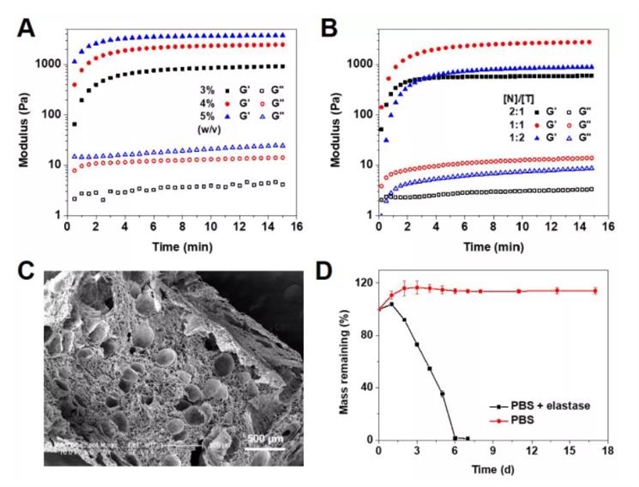
图1:(A) 聚合物浓度为 3%、4%、5% (w/v),[N]/[T] 为 1:1,(B) 聚合物浓度为 4% (w/v),[N]/[T] 为 2:1、1:1、1:2时,水凝胶的储能模量 (G´) 和损耗模量 (G") 随时间的变化。(C) 点击聚氨基酸水凝胶的 SEM 图像。(D) 含或不含 5 U/mL 弹性蛋白酶的 PBS 中水凝胶的体外降解曲线。
要点2:载 CDDP 的水凝胶体外释放分析
负载 CDDP 的水凝胶的流变测试表明凝胶化速率降低。如图2B所示,当 CDDP 与 PLG-Norb 骨架结合时,由于空间位阻增加,G´需要更长的时间才能达到相同的值。CDDP 从水凝胶的体外释放曲线在 37°C 的 PBS 中进行评估。在 12 天的测试期间,由于从 PLG-Norb 的羧基到氯离子的配体交换,34% 的 CDDP从水凝胶中持续释放出来 (图2C)。相比之下,在不含 NaCl 的 PB 中,只有 6.7% 的 CDDP 从水凝胶中释放出来。
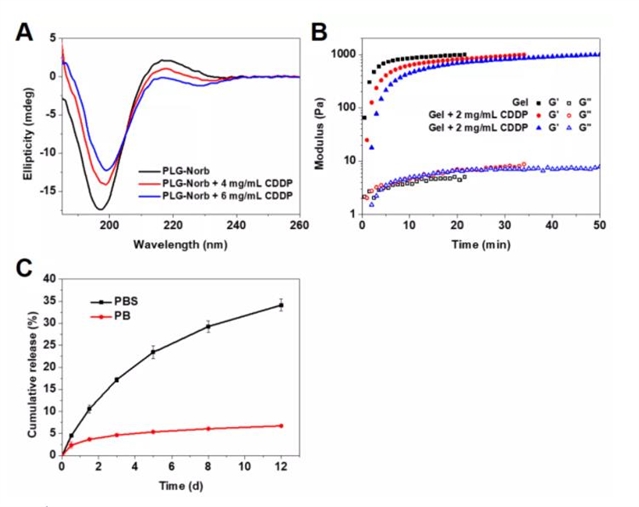
图2:(A) 在 5 mM PB (pH 7.4) 中聚合物浓度为 0.01 mg/mL 时的 CD 光谱。(B) 顺铂 (CDDP) 负载水凝胶的凝胶动力学,CDDP 浓度为 2 和 3 毫克/毫升。(C) 在 PBS 或 PB (不含 NaCl) 中,CDDP 从水凝胶中的体外释放曲线。
要点3:负载 CDDP 的水凝胶体外细胞学分析
使用 MCF-7 细胞评估了负载 CDDP 的水凝胶的体外肿瘤细胞抑制效率。如图 3A 所示,水凝胶本身没有表现出可检测到的细胞毒性,细胞活力保持在 95% 以上。相比之下,载有 CDDP 的水凝胶以剂量依赖性方式抑制 MCF-7 细胞的增殖。孵育 24 小时后,细胞活力从 90.7% 降低到 41.0%。由于 Pt 复合物的持续释放,增加孵育时间进一步增强了负载 CDDP 的水凝胶的抗肿瘤作用。如图3B所示,与 PBS 组 (38.35%) 相比,负载 CDDP 的水凝胶诱导 MCF-7 细胞的 S 期停滞 (50.10%),而空白水凝胶孵育的 MCF-7 细胞在不同阶段的百分比与 PBS 组的相当。这进一步证明了基于 iEDDA 的聚氨基酸水凝胶的细胞相容性。
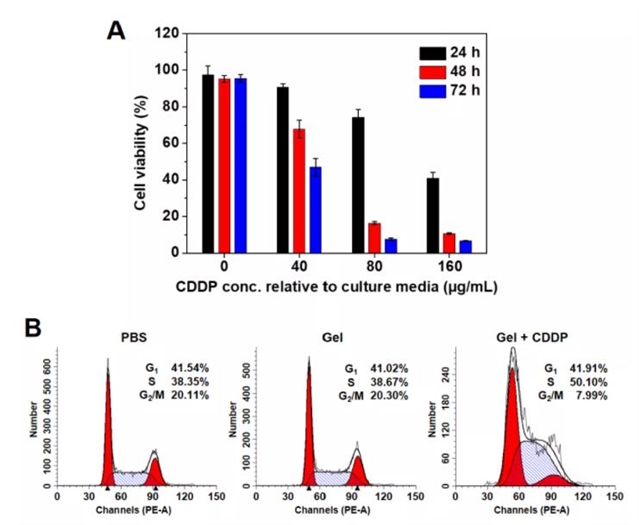
图 3. (A) 载有 CDDP 的水凝胶对 MCF-7 细胞的体外细胞毒性。(B) 由载有 CDDP 的水凝胶诱导的 MCF-7 细胞的细胞周期分布的流式细胞仪分析。
要点4:水凝胶的体内生物相容性分析
为了研究无铜点击聚氨基酸水凝胶的体内生物相容性,将 PLG-Norb 和 4aPEG-T 的 PBS 溶液在混合后皮下注射到大鼠背部。在不同的时间点处死大鼠并通过手术解剖注射部位以暴露水凝胶与相邻皮肤。据观察,水凝胶可以在注射部位形成而不会外渗到周围组织中。由于降冰片烯和四嗪基团之间的反应形成了稳定的共价键,4 周内水凝胶保持其结构完整性,并且发现在水凝胶周围形成薄的纤维囊 (图4)。此外,通过 H&E 和 Masson 三色染色处理水凝胶周围的宿主组织评估炎症反应。注射后1周,观察到炎症细胞增多,胶原沉积增多,显示初期为急性炎症反应。之后,炎症细胞逐渐减少。实验过程中未观察到肉眼可见的水肿、充血和组织坏死。因此,结果表明水凝胶具有良好的稳定性和组织相容性。
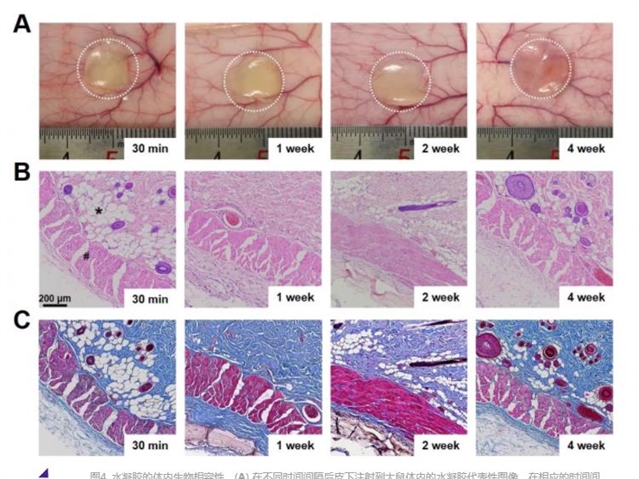
图4. 水凝胶的体内生物相容性。(A) 在不同时间间隔后皮下注射到大鼠体内的水凝胶代表性图像。在相应的时间间隔后水凝胶和周围组织的 (B) H&E 染色和 (C) 马森三色染色。星号表示水凝胶的位置。
要点5:载有 CDDP 的水凝胶的体内抗肿瘤功效分析
为了评估体内抗肿瘤功效,小鼠在第 0、3、7 天接受了 3 次游离 CDDP 瘤周注射,每次剂量为 3.3 mg/kg。如图 5A 所示,在 PBS 组中,肿瘤大小在实验过程中迅速增加。相比之下,游离 CDDP 和负载 CDDP 的水凝胶组的肿瘤生长得到有效抑制。值得注意的是,负载CDDP的水凝胶的抑制作用可以通过将剂量增加到15 mg/kg来进一步提高,TIR显着提高了86.6%。此外,通过监测小鼠体重来评估治疗的全身毒性。结果表明,即使 CDDP 剂量达到 15 mg/kg,用负载 CDDP 的水凝胶治疗的小鼠仍保持稳定的体重,表明基于水凝胶的治疗的全身毒性较低 (图5B)。进行H&E染色以评估各组中肿瘤和主要器官的组织学特征。如图5C所示,在PBS组的肿瘤组织中观察到紧密堆积的肿瘤细胞,表明肿瘤快速生长。化疗药物治疗后,细胞密度下降,出现不同程度的坏死区。另一方面,载有CDDP的水凝胶组动物的主要器官未观察到组织病理学变化。这证实了通过从肿瘤部位的水凝胶局部和持续释放 CDDP 进行治疗的低毒副作用。相比之下,游离 CDDP 引起明显的肾毒性,表现为肾囊腔收缩 [3]。
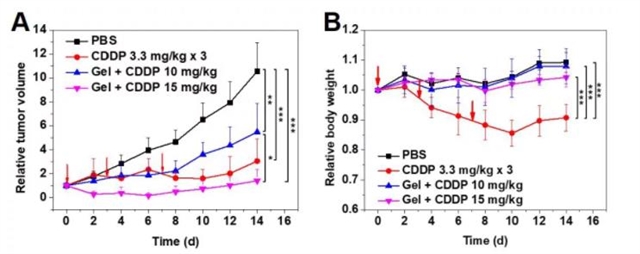
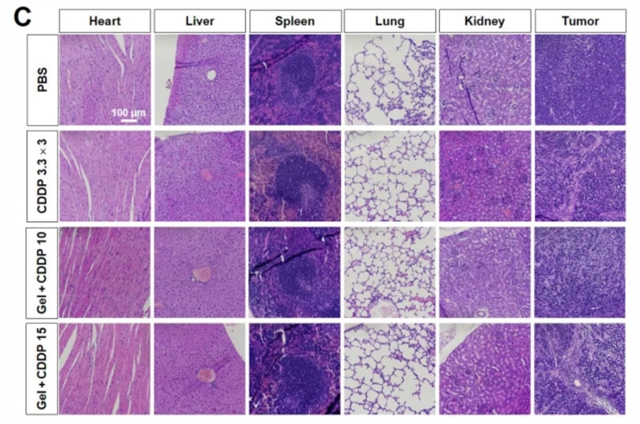
图5. 载有 CDDP 的水凝胶治疗携带 MCF-7 异种移植瘤的 BALB/c 裸鼠的体内抗肿瘤功效。(A) 相对肿瘤体积。(B) 相对体重。箭头表示在第 0、3、7 天以 3.3 mg/kg 的剂量注射 3 次游离 CDDP。数据表示平均值 ± SD;值通过单向方差分析,* p < 0.05,** p < 0.01,*** p < 0.001。(C) 第 14 天小鼠肿瘤组织和主要器官的 H&E 染色。
研究总结
在本研究中,通过 PLG-Norb 和 4aPEG-T 之间的 iEDDA 反应开发了一种可注射的聚氨基酸水凝胶,用于 CDDP 的局部递送。快速和生物正交的点击反应使我们能够制备具有不同机械性能的水凝胶。PLG 的羧基用于与 CDDP 形成聚合物 - 金属络合,延长释放曲线。对于携带 MCF-7 异种移植瘤的小鼠的体内治疗,由于肿瘤部位局部、持续的 CDDP 释放,单次瘤周注射负载 CDDP 的水凝胶表现出显着的抗肿瘤功效和降低的全身毒性。此外,点击水凝胶具有较小的炎症反应和良好的体内稳定性,是有吸引力的长效缓释材料。总体而言,可注射点击聚氨基酸水凝胶显示出作为局部、持续递送抗肿瘤药物平台的巨大潜力。
参考文献:
1. Wang, D.; Lippard, S.J. Cellular processing of platinum anticancer drugs. Nat. Rev. Drug Discov.2005,4, 307–320.
2. Ko, D.Y.; Shinde, U.P.; Yeon, B.; Jeong, B. Recent progress of in situ formed gels for biomedical applications. Prog. Polym. Sci.2013,38, 672–701.
3. Wu, X.; Wu, Y.; Ye, H.; Yu, S.; He, C.; Chen, X. Interleukin-15 and cisplatin co-encapsulated thermosensitive polypeptide hydrogels for combined immuno-chemotherapy. J. Control. Release2017,255, 81–93.
Polymers(ISSN 2073-4360,IF 4.329) 是一个国际型开放获取英文学术期刊,研究范围涵盖与聚合物研究相关的各个方面。Polymers目前已被SCIE、Scopus、PubMed等重要数据库收录。期刊采用单盲高标准同行评审制,一审周期平均为11.5天,文章从接收到发表平均仅2.7天。


特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。