|
|
| 深海真菌的新蛇孢菌素类化合物及其抗炎活性 | MDPI Marine Drugs |
|
论文标题:New Ophiobolins from the Deep-Sea Derived Fungus Aspergillus sp. WHU0154 and Their Anti-Inflammatory Effects
期刊:Marine Drugs
作者:Wenjuan Ding et al.
发表时间:20 November 2020
DOI:10.3390/md18110575
微信链接:
https://mp.weixin.qq.com/s?__biz=MzI1MzEzNjgxMQ==&mid=2649985052&idx=1&sn=
0a5ba9bc6785b37748ee10ea88bf10dc&chksm=f1de2ad8c6a9a3ce3521a259b4025485
2b299d22d367e757793987b562cef2c44c756ecb4f0b&token=799446241&lang=zh_CN#rd
期刊链接:https://www.mdpi.com/journal/marinedrugs
原文通讯作者简介

唐金山
暨南大学
唐金山,暨南大学药学院中药及天然药物研究所研究员、博士生导师。主要从事中药及天然药物 (包括海洋微生物) 活性物质的发现及其结构修饰研究。承担国家重点研发计划、国家自然科学基金及广东省自然科学基金等项目。
原文通讯作者简介

洪葵
武汉大学
洪葵,武汉大学药学院教授,主要从事海洋微生物新药发现研究,包括药用微生物资源收集与优选、基于基因组的天然产物发现、二倍半萜化合物生物合成机制及成药性评价。承担了国家重点研发计划、国家自然科学基金及欧盟第七框架、中泰合作等项目。
引言
深海具有高盐、高压、寡营养和低温等极端环境特征,近年来从深海真菌中发现了系列结构独特、多样,具有良好药理活性的天然产物,引起了研究人员从这种极端环境微生物中探索新化学实体的广泛兴趣。萜类化合物是重要的天然产物,至今发现10万多种,但二倍半萜只占不到2%,是稀有的萜类。蛇孢菌素(Ophiobolin) 是以相连的[5,8,5]环为基本骨架的二倍半萜类化合物,自1957年第一个蛇孢菌素Ophiobolin A作为一种植物毒素被发现,目前此类同系物约有70余种。蛇孢菌素具有广泛的生物活性,包括抗肿瘤、抗菌、抗炎和钙调神经磷酸酶抑制作用等。其结构和生物活性多样性引起了合成化学家和药理学研究者们的极大关注。
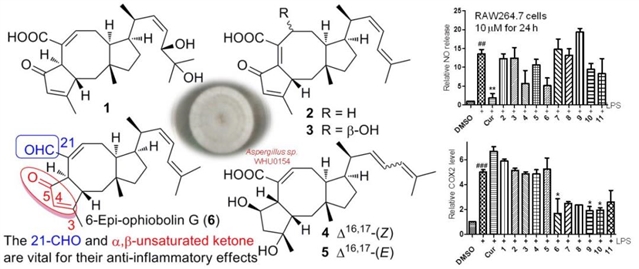
实验过程
武汉大学洪葵教授课题组从我国南海 (117°51.41E, 19°50.71N) 3197m深度的沉积物样品中分离到真菌WHU0154。根据其分生孢子形态学结构特征和转录间隔 (ITS) 序列鉴定该菌株为曲霉属真菌。通过对该菌株发酵粗提取物进行抗菌活性筛选和HPLC化合物初筛,发现其具有抗金黄色葡萄球菌ATCC5165活性及系列紫外吸收峰,选定该菌株为具有活性化合物合成能力的优质菌株。暨南大学团队接着利用PDA液体培养基对菌株进行16 L大量发酵,采用乙酸乙酯分别萃取发酵液并浸泡菌丝体,合并提取液后减压浓缩得到3.7 g提取物。综合运用各种色谱学分离方法和现代波谱学技术分离并鉴定了11个蛇孢菌素类化合物(图1),结合NMR图谱分析和实验、计算ECD等方法确定了新化合物的相对和绝对构型,其中5个为新化合物 (1-5)。
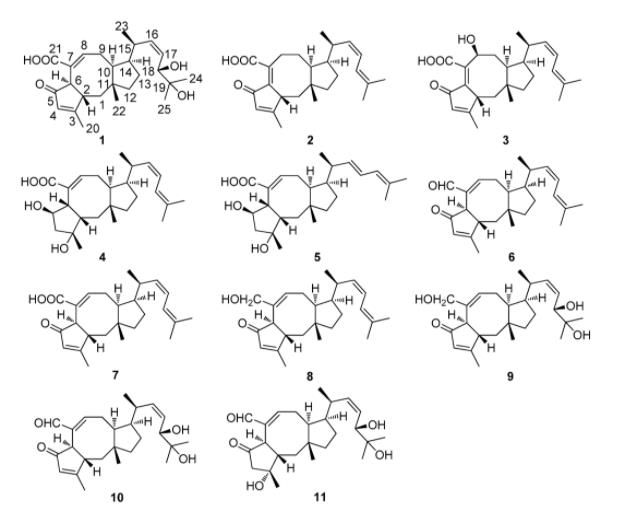
图1. 从深海真菌Aspergillussp. WHU0154发酵产物中分离的蛇孢菌素类化合物。
暨南大学团队接着对化合物1-11的抗炎活性进行了评价,并对其构效关系进行了初步探讨。通过检测化合物对脂多糖 (LPS) 诱导的小鼠单核巨噬细胞RAW264.7一氧化氮 (NO) 产生的影响 (姜黄素cur为阳性对照,DMSO为空白对照),发现化合物4和6对LPS诱导的RAW264.7细胞NO的释放有明显的抑制作用 (图2A),且在相应浓度下无明显细胞毒性 (图2B)。进一步抗炎机制研究表明,化合物6能够通过抑制iNOS蛋白表达来抑制LPS诱导的RAW264.7细胞中NO的产生(图2C、2E)。此外,化合物6、9和10还能抑制LPS诱导的RAW264.7细胞中与炎症相关的环氧化酶COX 2的表达(图2C、2D)。构效关系分析表明,蛇孢菌素中C-21位的醛基对其抗炎活性至关重要;此外,A环中α,β不饱和酮也可能是该类物质抗炎作用的关键药效团。
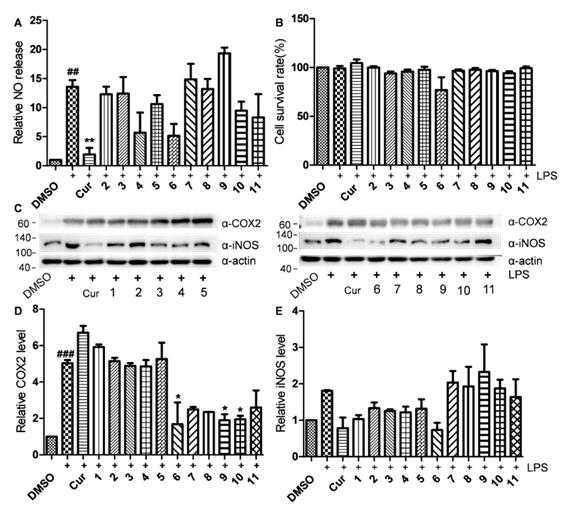
图2. 蛇孢菌素1-11抗炎活性及其初步机制研究。
总结
该研究工作从我国南海深海来源的一株曲霉属真菌Aspergillus sp.中分离鉴定了5个新的蛇孢菌素类化合物,首次探讨了它们抗炎作用的构效关系和初步作用机制。结果发现蛇孢菌素中C-21位的醛基和A环的α,β不饱和酮结构可能是该类化合物抗炎作用的关键药效团。该研究结果丰富了深海海洋真菌次级代谢产物的研究内容,为蛇孢菌素类化合物的进一步药物化学研究提供了理论基础和依据,并有助于发现新的、高效的抗炎剂。
该研究成果以“New Ophiobolins from the Deep-Sea Derived FungusAspergillus sp. WHU0154 and Their Anti-Inflammatory Effects”为题,发表于化学药物类期刊Marine Drugs(DOI: 10.3390/md18110575)。暨南大学研究生丁文娟、王方方和博士后Chokkalingam Uvarani为共同第一作者,暨南大学唐金山研究员和武汉大学洪葵教授为共同通讯作者。研究工作得到了国家重点研发计划(2018YFC0311000) 资助。
期刊简介
Marine Drugs(ISSN 1660-3397; IF4.073) 是国际型开放获取期刊之一,主题涵盖所有来自海洋活性物质的研究,涉及其发现、鉴定及各方面的应用。Marine Drugs目前已被SCIE、Scopus等重要数据库收录。采取同行评审,一审周期约为12.3天,文章从投稿到发表平均处理时间仅需33天。


特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。