2024年12月,西湖大学理学院叶宇轩课题组在Nature Chemistry上发表了一项研究:他们突破传统,让一类叫做烯还原酶的蛋白质“逆转”了自身的使命:烯还原酶的天然任务是还原,也就是把分子里碳和碳之间的双键变成单键,叶宇轩让它做了相反的事:从单键出发,造出双键。
但那时烯还原酶面对的,还是一张简单的地图。真实的合成场景,远比之来得复杂。
一年后,叶宇轩课题组带着同一支酶又来了。这一次,他们面对的是一个真正复杂的底物体系,而团队的目标也更具挑战:不仅要发生反应,还要精确决定反应发生的位置。
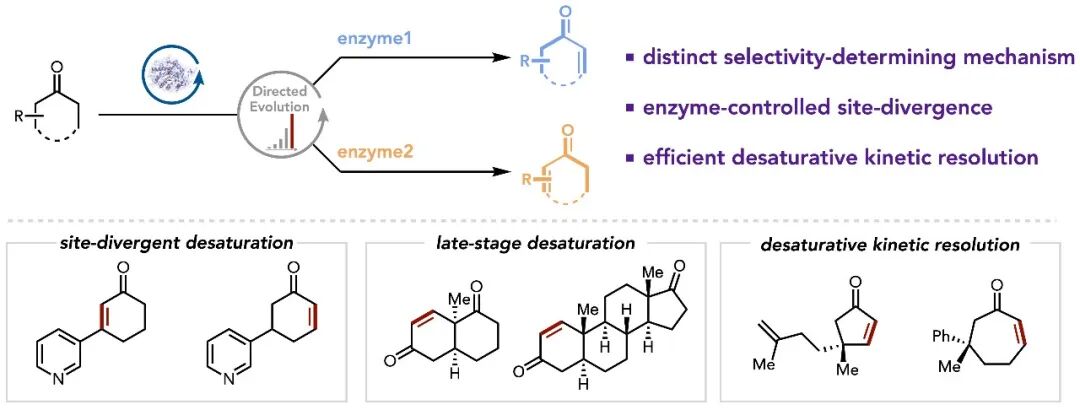 用于复杂分子后期修饰的酶催化选择性去饱和化
用于复杂分子后期修饰的酶催化选择性去饱和化
烯还原酶又一次漂亮地完成了任务。看完文章,也许你会感到,自然所蕴藏的可能性着实超过我们的想象。
这项研究,于近日再次发表在Nature Chemistry上。
选择困难
叶宇轩的这两项研究,最终产物都是烯酮(α,β-不饱和羰基化合物)。
烯酮的结构特征是:羰基(碳氧双键)旁边,挨着一个碳碳双键。正是这个双键组合,让它同时拥有两种截然相反的身份。
一方面,这类分子的化学结构极为活泼,像一个到处找人握手的“社牛”,很容易和周围富含电子的分子结合。一旦人体内的DNA和蛋白质与之握手,就可能带来毒性风险。
另一方面,烯酮也是药物设计里的重要结构单元。同样因为活泼,它可以主动锁住致病蛋白上的特定位点,形成共价结合。这类设计思路已经在抗癌药物开发中广泛使用。
同一个特性,放错地方是毒,用对了就是药。
正因如此,合成烯酮成为有机化学里的核心需求之一。化学家对此最直接的方法是脱氢:从一个普通的酮出发,在碳碳之间引入一个双键,造出烯酮。
这听起来简单,但在复杂分子上如何制造烯酮,这一步可以说难得出奇。
难处在于选择。
复杂的底物分子,它们的碳骨架绕来绕去,上面挂着各种官能团。可以脱氢的位置往往不止一个,而你需要在其中一个位置精确操作。
问题是,传统的化学方法很难分清差异。
就像一栋楼,每一层都有窗户,你现在要在三楼左侧第二个窗户上安装一扇玻璃,但你的工具,会同时对所有窗户起作用。
叶宇轩介绍,在多数传统催化体系中,催化剂能感知到的,常常是它正在操作的那个碳原子附近(α位)的化学环境——就像近视的你,只能看到眼前两米。但如果取代基位置稍远(β位甚至γ位),催化剂就会失去感知能力,反应究竟发生在哪里,往往难以精确控制。
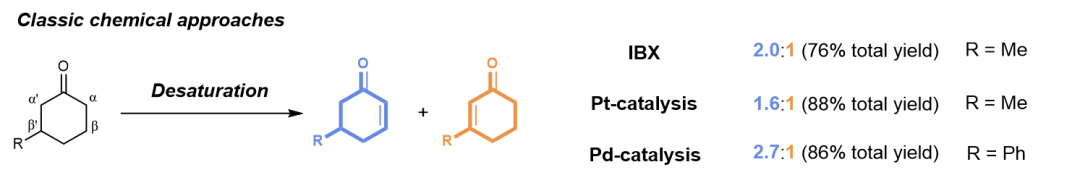 传统化学方法催化β-取代环己酮去饱和化结果
传统化学方法催化β-取代环己酮去饱和化结果
换句话说,化学催化剂在复杂分子中,往往会面临“选择困难症”。为了完成相应的合成目标,化学家经常需要大量的“绕路”工作,因此,整体的合成链条可谓繁复。
叶宇轩这项研究,就给这类问题提供了个新思路:直接换工具。
更大的地图
烯还原酶(EREDs)是叶宇轩选择的工具。
 实验室使用的烯还原酶
实验室使用的烯还原酶
在烯还原酶家族中,有一类成员叫做OYE——“老黄酶”(Old Yellow Enzyme),一个听上去非常老派的名字。名称来自其标志性的黄色,那是辅因子核黄素(维生素B2)的颜色。老黄酶是生物体防御系统的一部分,它的天职,是把有毒的烯酮还原掉。
叶宇轩的前一篇研究,就是证明通过改造,可以让它的逆反应变得高效可用。
这次,叶宇轩把同样的体系搬上了一张更大的地图。
当此次的底物从对称变成了不对称,听起来只是一个词的差别,但对催化剂的要求却完全不同。
来解释一下此时发生了什么:当底物对称,就意味着只有一个脱氢位点,自然不存在“哪里脱”的问题。但真实的合成场景里,分子往往长得不那么规整:一侧多了个取代基,两侧便不再等价,可以脱氢的位点随之变成了至少两个。
更进一步,不对称的底物本身就有手性,所以原料是两种镜像形式的混合物,潜在的选择位点进一步增加。要从多种可能性里精准选出一种,难度自不同日而语。
那么,老黄酶这次是如何做到的?
答案藏在反应机理的细节中。简单理解,关键并不在于酶“更强”,而在于它“看得更远”。
叶宇轩从上一篇研究中发现,老黄酶所感知并做出区分的,是β位的化学环境,而不是α位。
如前所述,传统化学催化往往依赖邻近环境作出判断。而酶则不同。众所周知,它是一个三维的蛋白质口袋,能够“囫囵吞枣”一般,把整个底物分子包裹在活性位点之中,因而可以感知β位、甚至更远处的空间信息。
更重要的是,叶宇轩发现,决定反应发生位置的,也是反应的第二步:β位氢负转移,这一步对底物构型与局部环境极为敏感,因此酶能够区分看似相似的不同位点。
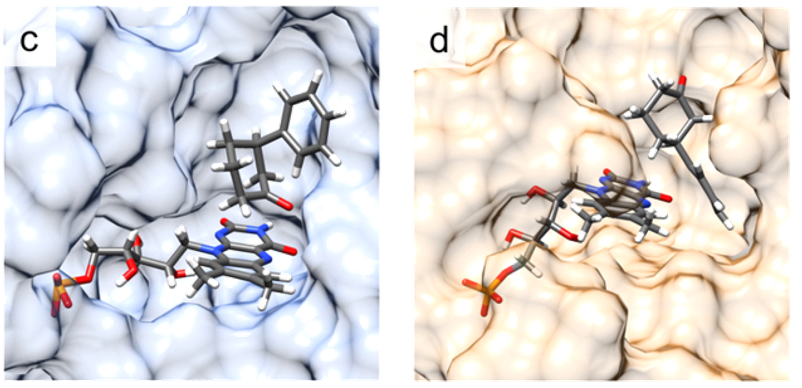 基于GkOYE与GsOYE优势变体对β-苯基环己酮底物的动力学模拟
基于GkOYE与GsOYE优势变体对β-苯基环己酮底物的动力学模拟
基于这一理解,叶宇轩课题组对老黄酶进行了改造,最终,他们实现了一种此前难以做到的能力:在同一个底物上,通过不同的酶,引导脱氢反应发生在不同的位置。化学上,这叫做“位点发散性去饱和化”。
对于一个已经被人类研究接近100年的老黄酶来说,这颇有些老树开新花的意味。
基于此,叶宇轩实现了在复杂分子上“定制化”地引入双键。这一系列研究,有望帮助科学家缩短合成路线、提高合成效率,加速新药分子的测试研发工作。
此外,他们还证明,酶催化与传统化学催化方法,并非简单的替换关系。
他们选择了萜类天然产物进行测试。这是一大类结构复杂的天然分子,诸如青蒿素、紫杉醇、薄荷醇、樟脑,都是萜类化合物。它们的碳骨架复杂,反应位点众多。
研究团队发现,在同一个底物上,传统化学方法倾向于在3a、4位发生脱氢;而酶催化体系,则更倾向于在6、7位进行反应。
两种工具就这样各自到达了对方触及不了的地方。
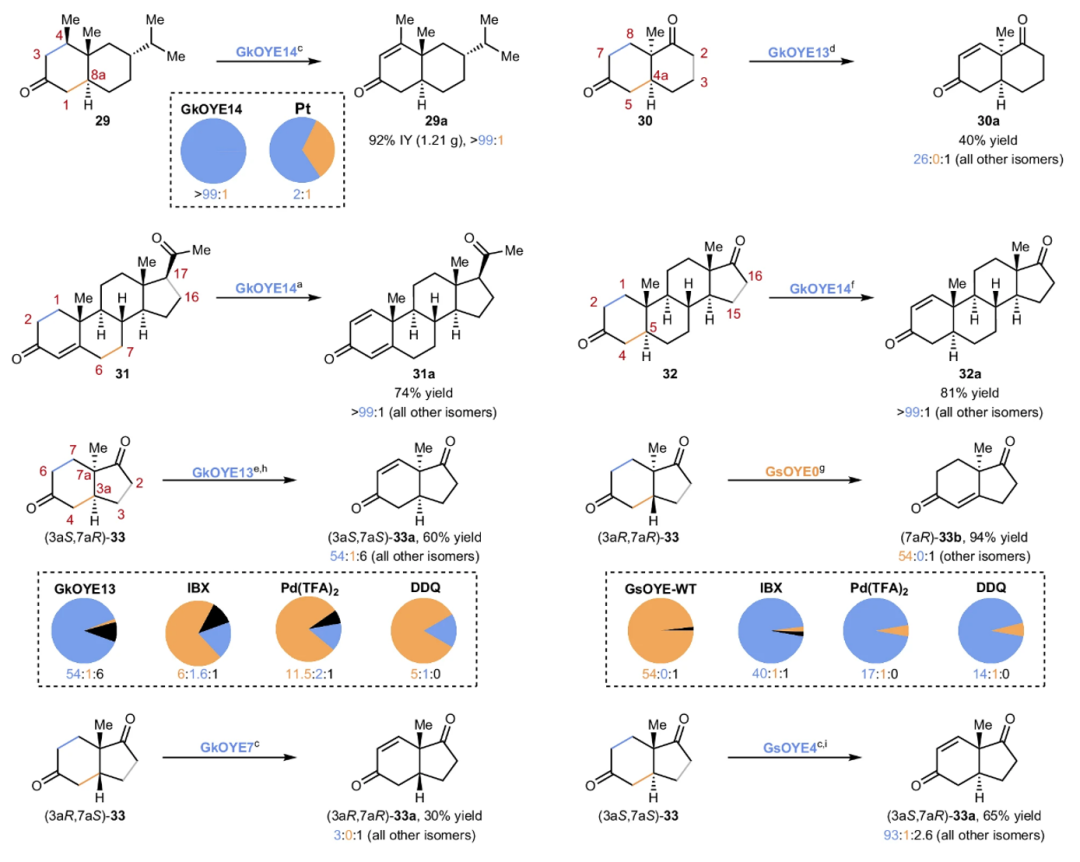 酶催化萜类分子位点选择性脱氢结果
酶催化萜类分子位点选择性脱氢结果
定向进化
那么,究竟叶宇轩是如何在烯还原酶身上,完成这样“逆天”的改造的?
讲起来好像很简单粗暴:"快速进化就行。"
叶宇轩说的是定向进化。
酶的功能由它的氨基酸序列决定,而氨基酸序列又由DNA编码。通过人为引入突变,可以获得一系列略有差异的酶变体。再通过筛选,挑选出表现更好的个体,作为下一轮进化的起点。
一轮接一轮,就像一场有方向的赛跑,最终跑向科学家所设定的终点。
“很多化学的方法,可以初步控制选择性,但很多时候不知道怎么提高、怎么优化。而酶不一样,你只要有一点能力,就可以快速进化。”
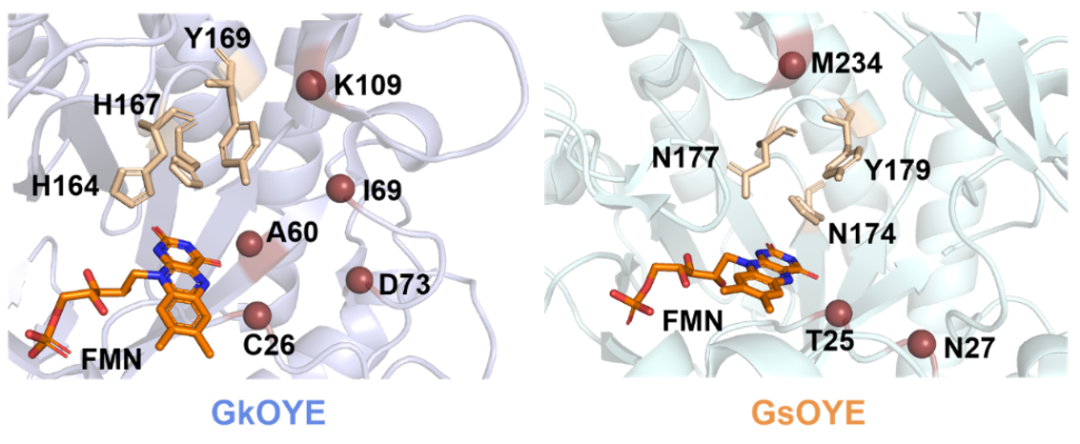 GkOYE与GsOYE酶活性中心关键氨基酸残基
GkOYE与GsOYE酶活性中心关键氨基酸残基
2018年,美国化学家Frances Arnold因定向进化的开创性工作获得诺贝尔化学奖。评奖词写道:它将达尔文的进化原理引入了试管之中。
进化论,在生命史上已经被验证了38亿年。定向进化,则是把亿万年的时间,压进了实验室一轮轮的进化周期里。因而,我们能够设定筛选标准,让迭代自己找到答案。
叶宇轩强调,定向进化的前提,“是这个蛋白质必须要有一点点这个能力”。
大众对酶有一个根深蒂固的印象:特异性极强,只做一件事。
但不是所有酶都如此。老黄酶的天然职责,是参与体内的氧化还原过程,其功能本身即有一定的广谱性。正是这种“并不完全专一”的特性,使它成为一个可以被重新训练的起点。
“大家现在也开始慢慢突破对酶的固有印象,酶能做的事情比我们想象得更多。”叶宇轩表示。
围绕烯还原酶去饱和化能力的这项研究,已经引起了工业界的注意。当前,叶宇轩课题组已与国外一家酶工业化应用企业签署了合作协议。
做出这样的研究选择,对叶宇轩来说,并非偶然。这本身就需要一种跨越学科边界的眼光。
“做酶的人知道这个酶可以做脱氢,但他也许不知道烯酮有用,”叶宇轩在采访中说,“做化学的知道烯酮有用,但他不知道酶可以做这件事。”
同时看到两边的故事,真正的机会往往就出现在二者之间的空白地带。叶宇轩自己的本科与博士阶段都在做有机化学,博后时期转向酶催化,这种跨越,让他能够同时看到两种体系的边界。
而交叉的结果便是,化学家们的工具箱里,又多了一件未曾有过的东西——一件大自然用38亿年打磨出来的工具。
 叶宇轩课题组合影
叶宇轩课题组合影
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。