|
|
|
|
|
中国科学家对映选择性合成季碳手性中心腈类化合物取得新进展 |
|
|
2021年11月4日,四川大学冯小明课题组(化学实验部分)与深圳湾实验室吴云东课题组(理论计算部分)合作,在J. Am. Chem. Soc.上发表了一篇题为“Enantioselective Synthesis of Nitriles Containing a QuaternaryCarbon Center by Michael Reactions of Silyl Ketene Imines with 1-Acrylpyrazoles”的新研究。
研究组使用手性双氮氧/钴(II)配合物(冯催化剂)作为催化剂,催化烯酮亚胺(Silyl Ketene Imines,简称SKIs)和α,β-不饱和吡唑酰胺的不对称Michael反应,合成了一系列含有季碳手性中心的腈类化合物。论文通讯作者是冯小明,刘小华,吴云东;第一作者是陈龙,蒲茂坪。
当一个碳原子上的氢原子被四个不同的碳基团取代时,即产生一个全碳季碳手性中心。与相应的叔碳手性中心相比,季碳手性中心更具有结构多样性和刚性,因此广泛存在于药物分子、天然产物和农用化学品中。由于受位阻拥挤、构象柔性的影响,构建季碳立体中心在有机合成中一直是一个巨大的挑战。烯酮亚胺(Silyl Ketene Imines,简称SKIs)是作为一个氰基阴离子等效体,目前已被用于多个不对称催化反应当中,由于SKIs和催化剂相互作用较弱,目前对SKIs的手性控制大部分仅限于非对映选择性控制,对于SKIs的直接对映选择性控制还没有报道,同1,2-加成相比较,在1,4-加成中,由于SKIs离催化剂较远,更是增加了催化剂对SKIs直接对映选择性控制的难度(图1)。
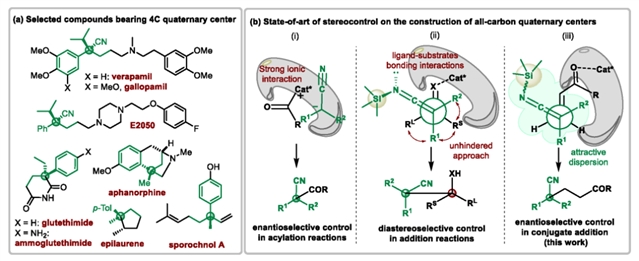
图1:(a)含有季碳手性中心的天然产物和药物;(b)SKIs不对称反应中的立体控制。
研究人员通过对反应溶剂、温度、金属等条件进行优化,尤其是对一系列手性双氮氧配体的筛选,最终在三氟甲磺酸钴(II)为中心金属,L-PrmtBu2为最优配体,水为添加剂,氯仿做溶剂,-60至-40℃的条件下高收率高对映选择性得到了含有季碳手性中心的腈类化合物(图2)。

图2:条件筛选
作者进行了底物普适性考察以及一系列衍生,并成功合成了(S)-verapamil、(S)-E2025、(S)-sporochnol A、(+)-glutechimide以及合成(−)-aphanorphine、(+)-epilaurene、(R)-aminoglutethimide等重要天然产物和药物分子的中间体(图3)。
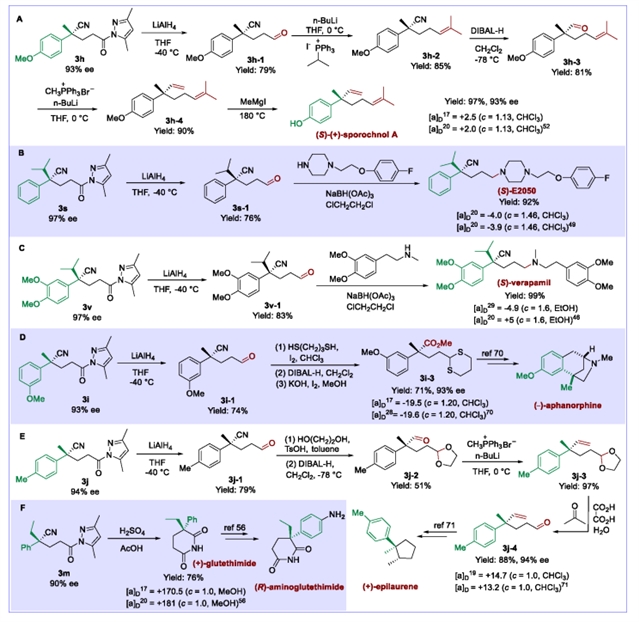
图3:产物衍生
为了理解手性双氮氧/钴(II)配合物催化SKIs和α,β-不饱和吡唑酰胺的不对称Michael反应的对映选择性调控机制,四川大学冯小明课题组与深圳湾实验室吴云东课题组合作,通过DFT理论计算发现,底物与配合物Int1的两种相互作用力:(a) SKIs的苯基与吡唑酰胺-Co(II)环之间的π-π相互作用;(b) C-H(SKI的苯基)与手性氮氧配体L-PrmtBu2的芳基的σ-π相互作用,在反应性和立体选择性方面起着关键作用(图4)。
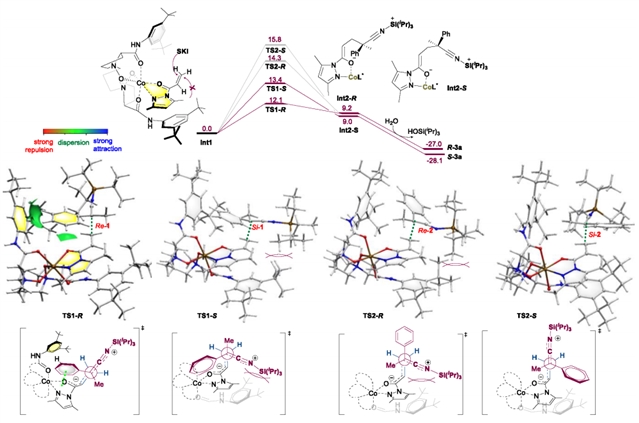
图4:DFT计算
本研究发展了手性双氮氧/钴(II)配合物(冯催化剂)催化SKIs与α,β-不饱和吡唑酰胺的不对称Michael反应,实现了对映选择性合成含有芳基、二烷基和氰基的季碳手性中心。该反应能在2.5 mol%催化剂条件下表现出广泛的底物兼容性。产物可用于多种手性药物和天然产物的合成。(来源:科学网)
相关论文信息:https://doi.org/10.1021/jacs.1c08382