近日,国际学术期刊Haematologica在线发表了中科院上海 研究院营养所王福俤研究组的研究论文Metalloreductase Steap3 coordinates the regulation of iron homeostasis and inflammatory responses。该研究结果揭示Steap3在巨噬细胞中发挥铁离子还原作用,Steap3缺失可影响巨噬细胞铁分布、造成细胞内可利用铁减少,从而影响TLR4介导的免疫炎症通路。
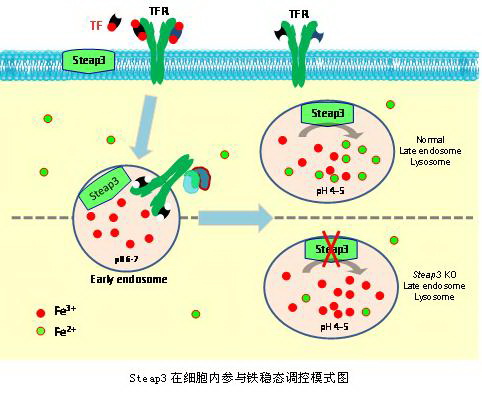
Steap3(Six-transmembrane epithelial antigen of the prostate 3)是2005年通过基因定位克隆技术(positional cloning)发现的一个影响机体铁代谢的基因,它含有具有还原活性的保守区域。哺乳动物主要由肠道吸收铁离子,之后三价铁离子进入血液与转铁蛋白(transferrin, Tf)结合形成Tf-Fe,Tf-Fe与细胞表面的转铁蛋白受体(transferrin receptor, TfR)结合,通过内吞进入细胞形成内含体(endosome)。而内含体膜上的铁离子通道DMT1和TRPML1只能往细胞质中运送二价铁离子,所以在内含体中铁离子有一个从三价到二价的还原过程,有研究提示Steap3在造血细胞内发挥金属还原酶作用,但Steap3在其它细胞内的功能和作用机制报道较少。
王福俤研究员指导的博士研究生张帆等利用Steap3基因敲除小鼠模型和原代培养细胞模型,发现Steap3在巨噬细胞中表达明显高于家族其它成员,同时在Steap3缺失的细胞中,铁离子有异常的分布及含量。在Steap3敲除巨噬细胞中,铁的还原活性明显降低,虽然和正常细胞相比含有相当量铁,但是其胞质内可利用的铁却明显少于正常细胞。Steap3敲除小鼠表现为小细胞贫血症状,脾脏肿大,血红蛋白和红细胞压积明显低于正常小鼠,但是血清铁含量却和正常小鼠相当,肝脏和脾脏铁甚至高于正常小鼠。这表明Steap3的缺失造成了细胞内及整个机体铁分布和代谢异常。
为了进一步研究Steap3是否在巨噬细胞免疫应答中起作用,研究人员用LPS分别刺激原代巨噬细胞和小鼠,结果发现,和STEAP其它家族成员相反,Steap3可以被LPS显著下调。而且Steap3敲除小鼠在LPS刺激下,血清铁没有像正常小鼠一样下调,肝脏和脾脏都比正常小鼠累积更多的铁,显示出异常的铁代谢。同时在Steap3敲除的巨噬细胞,LPS刺激后激活的由TLR4介导的Myd88非依赖性炎症通路明显减弱,这种减弱很有可能是由细胞内可利用铁减少引起的。
该研究首次发现Steap3参与巨噬细胞的铁离子还原作用,并揭示Steap3是介导铁代谢与免疫应答的重要分子,为进一步研究铁代谢与免疫应答之间的相互调节的机制研究提供了丰富的实验依据,也为铁代谢与免疫关系研究提供了新的线索。
该项工作得到了科技部、国家自然科学基金委、中国科学院及上海市科委等的经费资助。(来源:中科院上海 研究院)
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。