近日,四川农业大学动物医学院预防兽医研究所所长陈舜教授团队在npj Vaccines在线发表了题为《异位表达C蛋白的组装缺陷的坦布苏病毒是开发黄病毒的减毒活疫苗的新途径》的研究论文,报道了一种黄病毒通用的新型减毒活疫苗的制备策略。
登革病毒、寨卡病毒、日本乙脑病毒等,在世界范围多次引起公共卫生安全事件或威胁的人畜共感染的蚊媒病毒都属于黄病毒。由于没有特效抗病毒治疗药物,疫苗免疫仍是预防这类病毒性传染病的必须手段。早前,黄热病毒YF17D及乙型脑炎病毒SA-14-14-2弱毒疫苗的成功研发和应用,证明了减毒活疫苗是预防黄病毒感染的理想的疫苗开发重要途径。但减毒活疫苗的经典开发方法是通过连续盲传以获得无预期的自发突变,最终达到减毒的效果。由于其遗传背景不清晰,所以疫苗的工作原理和保护范围不明确,这就容易导致无法有效应对由特定黄病毒引起的突发的公共卫生事件。为了解决这个科学和应用问题,川农学者提出并探讨了人为定向地改变黄病毒结构蛋白的时序切割而致弱病毒的新策略。
新策略以禽坦布苏病毒作为黄病毒的研究模型,利用反向遗传操作技术,合理设计并成功获得了异位表达病毒的C蛋白,具有双顺反子基因组结构的重组病毒。该重组病毒由于病毒粒子的组装过程严重受损,因而在细胞上和动物体内毒力都显著减弱,感染动物后不引起任何临床症状。且单一剂量接种,便能完全保护动物在再次暴露于病毒感染后,不会产生任何明显临床症状,从而提供了更优的免疫保护效果。
此外,该策略未改变病毒抗原蛋白编码序列,能诱导忠实的免疫应答;而且,黄病毒的基因组结构和组装机制都十分相似,所以此减毒策略可作为黄病毒通用的减毒方案。加之,新策略利用反向遗传操作技术,可在数天内快速获得减毒活疫苗的候选株,在遇到由新型黄病毒引起的突发的公共卫生危机时,就能快速地做出应对,大大提高实际效益。因此,该新策略可广泛地适用于蚊媒黄病毒的弱毒疫苗株的快速培育,推进了疫苗方法学的理论创新。
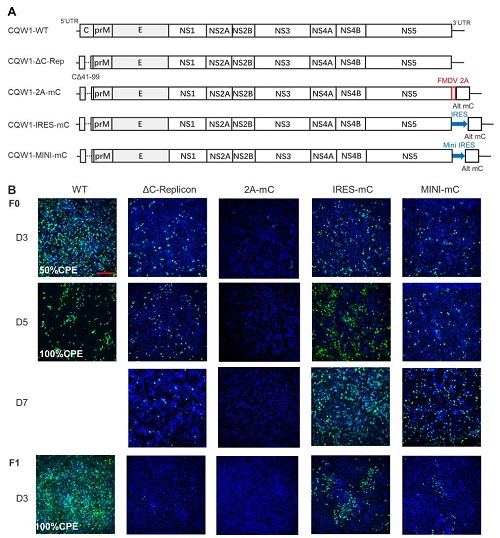
异位表达C蛋白的重组病毒的基因组示意图及拯救。 四川农业大学动物医学院供图
异位表达C蛋白的重组病毒的模型。 四川农业大学动物医学院供图
该研究得到了中国农业产业体系以及四川省兽药创新团队项目的支持。
相关论文信息:https://doi.org/10.1038/s41541-022-00468-y