|
|
|
|
|
阿尔兹海默症与长寿由同一关键因素影响 |
|
抑制它,或可延长寿命、预防阿尔兹海默症! |
阿尔兹海默症(AD)是最常见的神经退行性疾病之一,65岁以上的老年人中患病率通常为10%,85岁以上人群中患病率约为50%,目前还没有有效治疗阿尔兹海默症的方法。
正常衰老过程中的认知能力会下降,尽管老年人经常患阿尔兹海默症,但它并不是正常衰老的一部分,目前还不清楚导致阿尔兹海默症的确切原因。一些风险因素可能会使人更容易患阿尔兹海默症,而年龄是最突出的因素。最新发表的一项成果表明阿尔兹海默症和寿命长短是由同一因素决定。
北京时间3月31日凌晨,深圳理工大学讲席教授叶克强团队的最新研究成果发表于Science Advances。研究团队在以往的研究理论基础上,提出阿尔兹海默症与人的预期寿命均受大脑中的“C/EBPβ/AEP”神经信号通路影响。
阿尔兹海默症与衰老有共因
此前,叶克强团队基于过去十多年发表的上百篇论文,提出了一种全新的理论假设,这一假设认为:大脑中存在一条“C/EBPβ/AEP神经信号通路”,该通路的激活是导致阿尔兹海默症等神经退行性疾病的核心因素。
而这条影响阿尔兹海默症的神经信号通路,也影响着寿命的长短。其中,关键转录因子C/EBPβ发挥着重要作用。
C/EBPβ起着调节营养代谢、能量稳态和脂肪分化的作用,它能增加脑细胞中某些蛋白质的水平;而AEP是一种酶,它可将一些蛋白质剪切,这些片段逐渐聚集会引发阿尔兹海默症,逐步破坏患者的记忆和思维能力,最终影响其日常生活能力。
研究团队发现,C/EBPβ可能在决定寿命长短中发挥作用,它介导了多种与年龄相关的基因,并且其表达水平在老化的神经细胞中急剧升高。
为了探索C/EBPβ在衰老神经细胞中的作用,叶克强团队构建了一个小鼠模型,该模型可以选择性地在大脑神经元中过度表达C/EBPβ以模仿衰老的动物。研究发现小鼠的寿命以基因剂量依赖的方式发生变化。通常情况下,小鼠正常预期寿命为24-28个月,携带一份过表达C/EBPβ的小鼠寿命为12-18个月,两份为5-9个月,相比之下,减少一份 C/EBPβ基因表达可将寿命延长至 30 个月以上。此外,神经细胞中C/EBPβ过表达的小鼠表现出认知功能受损,类似于年迈大脑中的痴呆表现。
这说明,影响阿尔兹海默症的关键转录因子C/EBPβ,对寿命的长短也有影响,C/EBPβ基因表达越高的小鼠,寿命更短,而携带更少C/EBPβ基因的小鼠寿命则更长。
抑制AEP,延缓衰老
另一方面,研究者发现,C/EBPβ转基因小鼠表现出了显著的神经兴奋,这一现象与大量抑制性的GABA神经元损失有关。
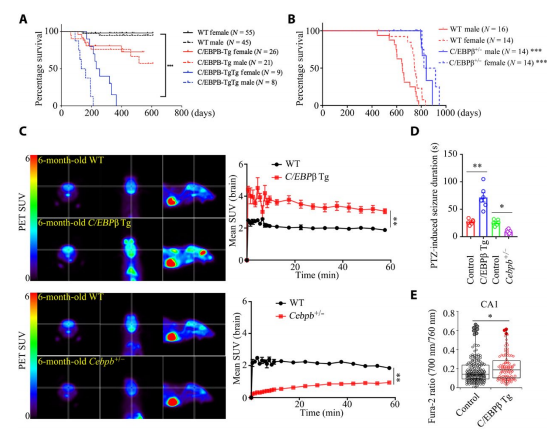
神经细胞中C/EBPβ升高引起神经兴奋,缩短小鼠生命周期
GABA是大脑中主要的抑制性神经递质,其缺失是阿尔兹海默症的重要临床症状。随着阿尔兹海默症的加重,大脑中的C/EBPβ/AEP含量会呈一定趋势升高,导致患者大脑中的GABA神经元选择性死亡。叶克强表示,阿尔兹海默症患者中GABA和GABA神经元的减少可能是神经过度活跃的原因,病人表现为癫痫发作,这与在 C/EBPβ转基因小鼠中观察到的情况类似。进一步表明,人类寿命和记忆储存与 C/EBPβ/AEP信号通路密切相关。
随着年龄的增长,人的大脑中的C/EBPβ的基因表达也会随之升高,60-84岁时达到顶峰,在85岁以上则下降。AEP作为C/EBPβ下游产物,两者趋势相似,更加长寿的寿星通常在神经细胞中会表达较少的AEP,而寿命稍短的个体表达较多的AEP基因。
在线虫的研究中,神经兴奋会随着年龄的增长而增加,而抑制神经兴奋可增加寿命。研究者发现,神经细胞中高表达C/EBPβ基因或AEP蛋白酶会缩短生命周期,而这些在肌肉中的高表达则没有影响。与小鼠类似,在线虫中敲除C/EBPβ或AEP则可延长生命周期。此外,研究者使用药物抑制线虫大脑中的AEP蛋白酶,延长了其生命周期,这表明特定药物制剂应该可适当减速衰老进程,延长寿命。
影响寿命的因素有很多。如限制食物摄取能够有效地延长哺乳动物生命周期;代谢的高低与寿命之间存在重要联系;科学研究表明,减少大脑内胰岛素信号传导,寿命增加。研究团队发现,C/EBPβ/AEP信号与人脑中的胰岛素信号呈负相关。在70-80岁的人中,胰岛素信号最低,C/EBPβ/AEP信号通路活跃达到顶峰。然而,在更加长寿的人中,C/EBPβ/AEP信号通路的活性下降,大脑中的胰岛素信号活性上升。
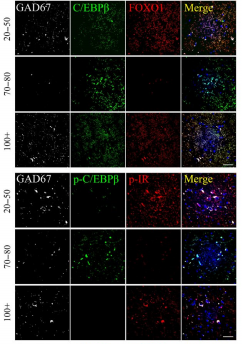
C/EBPb 调节人脑神经细胞中胰岛素及FOXO信号,以及调控生命周期
“此前我们的研究发现,C/EBPβ/AEP神经信号通路在驱动阿尔兹海默症中起着至关重要的作用,随着阿尔兹海默症病情的加重,C/EBPβ含量逐渐升高,FOXO1含量逐渐降低,这一全新发现将这一理论从阿尔兹海默症发病机制扩展到了对生命周期的调节。我们将进一步深入研究,以期通过药物抑制AEP治疗阿尔兹海默症患者,延缓衰老进程,延长人类寿命。”论文通讯作者叶克强表示。
论文链接:https://www.science.org/doi/10.1126/sciadv.abj8658
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。